
运用化学反应原理研究氮、氧、镁、铜等元素及其化合物的性质。
⑴合成氨反应反应:N2(g)+3H2(g)![]() 2NH3(g),ΔH=-QkJ/mol。若在恒温、恒压条件下向平衡体系中通入氩气,则该化学反应平衡移动 (填“向左”“向右”或“不”);使用催化剂可以加快反应速率,提高合成氨工业的氨气产量,则该反应的ΔH (填“增大”“减小”或“不改变”)。
2NH3(g),ΔH=-QkJ/mol。若在恒温、恒压条件下向平衡体系中通入氩气,则该化学反应平衡移动 (填“向左”“向右”或“不”);使用催化剂可以加快反应速率,提高合成氨工业的氨气产量,则该反应的ΔH (填“增大”“减小”或“不改变”)。
⑵在25℃下,将aL,0.01mol·L-1的氨水加入到1L,0.01mol·L-1的盐酸溶液中,若反应后溶液中c(NH4+)>c(Cl-),则溶液显____性(填“酸”“碱”或“中”)。若a>1,反应所得溶液中下列离子浓度比较可能正确的是
①Cl->H+>NH4+>OH-;②Cl->NH4+>H+>OH-;③Cl-=NH4+>H+=OH-;④NH4+>Cl->OH->H+
⑶在25℃下,向浓度均为0.1mol·L-1的MgCl2和CuCl2混合溶液中逐滴加入氨水,先生
成_______沉淀(填化学式),生成该沉淀的离子方程式为_________________________;继
续滴加氨水,最后一步发生的反应的离子反应方程式
参考数据:25℃,Ksp[Mg(OH)2]=1.8×10-11,KsP[Cu(OH)2]=2.2×10-20。
⑷有人设想寻求合适的催化剂和电极材料,以N2和H2为电极反应物,以HCl-NH4Cl为电
解质溶液环境制备新型燃料电池。则该燃料电池负极附近的pH____(填“增大”、“减小”或“不变”);正极的电极反应方程式为________ _____
科目:高中化学 来源: 题型:阅读理解
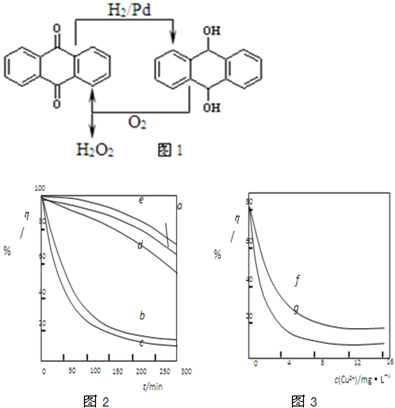
| ||
查看答案和解析>>
科目:高中化学 来源: 题型:
+ 2 |
- 6 |
+ 2 |
- 6 |
+ 4 |
| 10-9 |
| a-0.01 |
| 10-9 |
| a-0.01 |
查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解
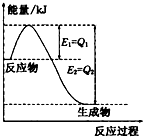 运用化学反应原理研究氮、氯、碘等单质及其化合物的反应有重要意义.
运用化学反应原理研究氮、氯、碘等单质及其化合物的反应有重要意义.
| ||
| (一定条件) |
| b×10-7 |
| a-b |
| b×10-7 |
| a-b |
查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解

| 10-7y |
| x-y |
| 10-7y |
| x-y |
查看答案和解析>>
科目:高中化学 来源: 题型:
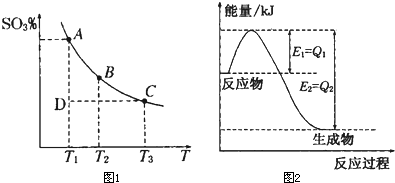
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com