
【题目】某课外活动小组的同学,在实验室做锌与浓硫酸反应的实验时,甲同学认为产生的气体是二氧化硫,而乙同学认为除二氧化硫气体外,还可能产生氢气.为了验证甲、乙两位同学的判断是否正确,丙同学设计了如图所示的实验装置(锌与浓硫酸共热时产生的气体为X,反应装置略去).

注:C中为氧化铜粉末,试回答下列问题:
(1)上述反应中生成二氧化硫的化学方程式为:________________________________;
(2)乙同学认为还可能产生氢气的理由是:____________________________________;
(3)丙同学在安装好装置后,必不可少的一步操作是:__________________________;
(4)A中试剂是______,D中试剂是______;
(5)E装置的作用是_________________________;
(6)可以证明气体X中含有氢气的实验现象是:______________________________。
【答案】 Zn+2H2SO4(浓)![]() ZnSO4+SO2↑+2H2O 浓H2SO4逐渐变稀,Zn与稀H2SO4反应可产生H2 检查装置的气密性 品红溶液 无水硫酸铜 防止空气中的水蒸气进入D中 C中黑色的固体变成红棕色,D中白色粉末变成蓝色.
ZnSO4+SO2↑+2H2O 浓H2SO4逐渐变稀,Zn与稀H2SO4反应可产生H2 检查装置的气密性 品红溶液 无水硫酸铜 防止空气中的水蒸气进入D中 C中黑色的固体变成红棕色,D中白色粉末变成蓝色.
【解析】(1)锌和浓硫酸反应是二氧化硫、硫酸锌和水,反应的化学方程式为Zn+2H2SO4(浓)![]() ZnSO4+SO2↑+2H2O;(2)由于反应时浓H2SO4浓度逐渐变稀,Zn与稀H2SO4反应可产生H2;(3)装置是气体验证实验,所以在安装好装置后,必不可少的一步操作是先检查装置的气密性;(4)分析装置图可知,生成的气体中有二氧化硫和氢气,所以装置A是验证二氧化硫存在的装置,选品红溶液进行验证;通过高锰酸钾溶液除去二氧化硫,通过装置B中的浓硫酸除去水蒸气,利用氢气和氧化铜反应生成铜和水蒸气,所以利用装置D中的无水硫酸铜检验水的生成,则D中试剂是无水硫酸铜;(5)为避免空气中的水蒸气影响D装置中水的检验,装置E中需要用碱石灰,目的是防止空气中的水蒸气进入D中;(6)氢气具有还原性,能把氧化铜还原为铜,则证明气体X中含有氢气的实验现象是C中黑色的固体变成红棕色,D中白色粉末变成蓝色。
ZnSO4+SO2↑+2H2O;(2)由于反应时浓H2SO4浓度逐渐变稀,Zn与稀H2SO4反应可产生H2;(3)装置是气体验证实验,所以在安装好装置后,必不可少的一步操作是先检查装置的气密性;(4)分析装置图可知,生成的气体中有二氧化硫和氢气,所以装置A是验证二氧化硫存在的装置,选品红溶液进行验证;通过高锰酸钾溶液除去二氧化硫,通过装置B中的浓硫酸除去水蒸气,利用氢气和氧化铜反应生成铜和水蒸气,所以利用装置D中的无水硫酸铜检验水的生成,则D中试剂是无水硫酸铜;(5)为避免空气中的水蒸气影响D装置中水的检验,装置E中需要用碱石灰,目的是防止空气中的水蒸气进入D中;(6)氢气具有还原性,能把氧化铜还原为铜,则证明气体X中含有氢气的实验现象是C中黑色的固体变成红棕色,D中白色粉末变成蓝色。


科目:高中化学 来源: 题型:
【题目】在氯水中存在多种分子和离子,它们在不同的反应中表现出各自的性质。下列实验现象和结论一致且正确的是
A. 加入有色布条,一会儿有色布条褪色,说明溶液中有HCl存在
B. 溶液呈黄绿色,且有刺激性气味,说明有Cl2分子存在
C. 加入硝酸酸化的AgNO3溶液产生白色沉淀,说明有Cl2存在
D. 加入Na2CO3溶液,有气泡产生,说明有HClO分子存在
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以冶铝的废弃物铝灰为原料制取超细α氧化铝,既降低环境污染又可提高铝资源的利用率。已知铝灰的主要成分为Al2O3(含少量杂质SiO2、FeO、Fe2O3),其制备实验流程如下: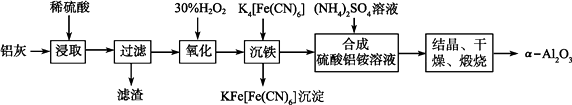
(1)写出铝灰与硫酸反应涉及的离子方程式。
(2)图中“滤渣”的主要成分为(填化学式)。
(3)加30%H2O2溶液发生的离子反应方程式为。
(4)煅烧硫酸铝铵晶体,发生的主要反应为:4[NH4Al(SO4)2·12H2O] ![]() 2Al2O3+2NH3↑+N2↑+5SO3↑+3SO2↑+53H2O,将产生的气体通过下图所示的装置。
2Al2O3+2NH3↑+N2↑+5SO3↑+3SO2↑+53H2O,将产生的气体通过下图所示的装置。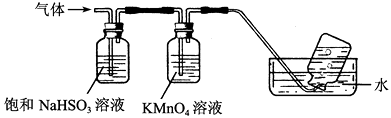
①集气瓶中收集到的气体是(填化学式)。
②足量饱和NaHSO3溶液吸收的物质除大部分H2O(g)外还有(填化学式)。
③KMnO4溶液褪色(MnO 被还原为Mn2+),发生的离子反应方程式为。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在密闭容器中充入4mol SO2和3mol O2 一定条件下建立平衡2SO2(g)+O2(g)═2SO3(g)△H=﹣Q KJ/mol,测得SO2的转化率为90%,则在此条件下,反应放出的热量为( )
A.1.8Q KJ
B.2Q KJ
C.Q KJ
D.0.9Q KJ
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用酸性氢氧燃料电池为电源进行电解的实验装置如图所示.下列说法中正确的是( ) 
A.燃料电池工作时,正极反应:O2+2H2O+4e﹣═4OH﹣
B.a极是铁,b极是铜时,b极逐渐溶解,a极上有铜析出
C.a极是粗铜,b极是纯铜时,随着反应的进行浓度减小
D.a、b两极均是石墨时,在相同条件下b极产生的气体与电池中消耗的H2体积相等
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com