
对下列事实的解释正确的是
A.浓硝酸通常保存在棕色的试剂瓶中,说明浓硝酸不稳定
B.浓硫酸具有吸水性,说明可用浓硫酸干燥氨气
C.足量铁与稀硝酸反应后溶液呈浅绿色,说明稀硝酸不能氧化Fe2+
D.常温下,可用铝制容器盛装浓硫酸,说明浓硫酸与铝不反应
科目:高中化学 来源:2015-2016学年吉林省高二上学期期中测试化学试卷(解析版) 题型:选择题
使1 mol乙烯的同系物丙烯与氯气完全发生加成反应,然后使该加成反应的产物与氯气在光照条件下发生完全取代反应,则两个过程中消耗氯气的总物质的量是
A.3 mol B.4 mol C.5 mol D.7 mol
查看答案和解析>>
科目:高中化学 来源:2015-2016学年吉林省高二上11月月考化学试卷(解析版) 题型:选择题
食物是维持人类生命和健康的支柱。下表是某食品包装袋上的说明:
品名 | 蔬菜苏打饼 |
配料 | 面粉、鲜鸡蛋、精炼食用植物油、白砂糖、奶油、食盐、脱水青菜、橙汁 |
保质期 | 十二个月 |
生产日期 | 2015年11月2日 |
对上表中各种配料成分的理解,不正确的是
A.含蛋白质的是鲜鸡蛋
B.含淀粉的是面粉和白砂糖
C.含油脂的是精炼食用植物油和奶油
D.含维生素的是脱水青菜和橙汁
查看答案和解析>>
科目:高中化学 来源:2015-2016学年四川省高一上期中测试化学试卷(解析版) 题型:选择题
下列说法正确的是
A.NaOH固体溶于水后能导电,所以NaOH溶液是电解质
B.H2SO4、Na2CO3、B(OH)2在水溶液中以离子的形式存在
C.液态氯化氢能导电,所以HCl是电解质
D.NH3溶于水能导电,所以NH3是电解质
查看答案和解析>>
科目:高中化学 来源:2016届甘肃省天水市高三上学期期中测试化学试卷(解析版) 题型:实验题
Ⅰ.硫酸工业产生的废气A(主要成分:SO2、O2、N2、CO2等)排放到空气中会污染环境。某化学兴趣小组对废气A的组成进行探究,请回答下列问题。
(1)同学甲设计实验检验废气A中含有CO2,应选择的试剂有 。
A.NaOH溶液 B.酸性KMnO4溶液 C.澄清石灰水 D.盐酸
(2)同学乙欲测定废气A中SO2的含量,取a L废气A并设计了如下装置进行实验。
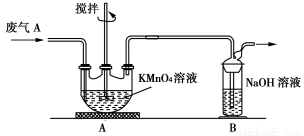
①为了保证实验成功,装置A应具有的现象是 ,搅拌的目的是 。
②同学丙认为A装置前后的质量差就是a L废气中含有的SO2的质量,然后进行含量计算。经小组讨论后,同学丁提出疑问,按照同学丙的实验,若废气中SO2完全被吸收,则最后测定的结果应该偏大,同学丁推断的理由是 。
Ⅱ.溴酸钾具有毒性,是一种常用的分析试剂和氧化剂,实验室中制备过程如下:
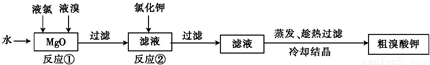
已知反应②是复分解反应,根据上述转化关系回答下列问题:
(1)反应①的化学方程式为 .
(2)反应②的化学方程式为 .
(3)现向含6mol KI的硫酸溶液中逐滴加入KBrO3溶液,整个过程中含碘物质的物质的量与所加KBrO3的物质的量的关系如图所示.请回答下列问题:
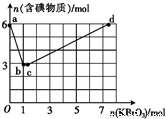
①已知b点时,KI反应完全,转移的电子数为 .
②b→c过程中,仅有一种元素的化合价发生了变化.则反应时氧化剂与还原剂的物质的量之比为 .
③d点时,n(KBrO3)为 .
查看答案和解析>>
科目:高中化学 来源:2016届山西省高三上学期10月月考化学试卷(解析版) 题型:选择题
下列有关硅及其化合物的说法中正确的是
A.在粗硅的提取中发生反应2C+SiO2=2CO+Si,硅被还原,所以碳的还原性大于硅的还原性
B.硅酸钠属于盐,不属于碱,所以硅酸钠可以保存在磨口玻璃塞试剂瓶中
C.用SiO2制取硅酸,应先使二氧化硅与氢氧化钠溶液反应,然后再通入CO2
D.由Na2CO3+SiO2 CO2+Na2SiO3可知硅酸的酸性大于碳酸
CO2+Na2SiO3可知硅酸的酸性大于碳酸
查看答案和解析>>
科目:高中化学 来源:2016届浙江省嘉兴市高三上学期期中测试化学试卷(解析版) 题型:填空题
工业生产硝酸铵的流程如下图所示
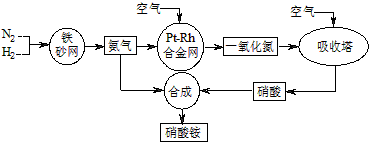
(1)硝酸铵的水溶液呈 (填“酸性”、“中性”或“碱性”);其水溶液中各离子的浓度大小顺序为: 。
(2)已知N2(g)+3H2(g) 2NH3(g) △H<0,当反应器中按n(N2):n(H2)=1:3投料,分别在200℃、400℃、600℃下达到平衡时,混合物中NH3的物质的量分数随压强的变化曲线如下图。
2NH3(g) △H<0,当反应器中按n(N2):n(H2)=1:3投料,分别在200℃、400℃、600℃下达到平衡时,混合物中NH3的物质的量分数随压强的变化曲线如下图。
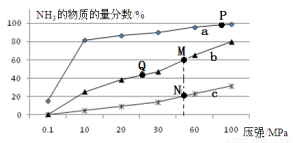
①曲线a对应的温度是 。
②关于工业合成氨的反应,下列叙述正确的是
A.及时分离出NH3可以提高H2的平衡转化率
B.P点原料气的平衡转化率接近100%,是当前工业生产工艺中采用的温度、压强条件
C.上图中M、N、Q点平衡常数K的大小关系是K(M)=K(Q)>K(N)
D.M点对应的H2转化率是75%
E.如果N点时c(NH3)=0.2 mol·L-1,N点的化学平衡常数K≈0.93
(3)尿素(H2NCONH2)是一种非常重要的高效氮肥,工业上以NH3、CO2为原料生产尿素,该反应实际为二步反应:第一步:2NH3(g)+CO2(g)===H2NCOONH4(s) ΔH=-272 kJ·mol-1
第二步:H2NCOONH4(s)===CO(NH2)2(s)+H2O(g) ΔH=+138 kJ·mol-1
写出工业上以NH3、CO2为原料合成尿素的热化学方程式:
(4)某实验小组模拟工业上合成尿素的条件,在一体积为0.5 L密闭容器中投入4 mol氨和1mol二氧化碳,实验测得反应中各组分随时间的变化如下左图所示:
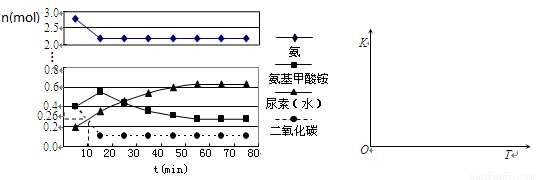
①已知总反应的快慢由慢的一步决定,则合成尿素总反应的快慢由第__________步反应决定,总反应进行到________min时到达平衡。
②反应进行到10 min时测得CO2的物质的量如图所示,则用CO2表示的第一步反应的速率v(CO2)=_______________mol·L-1·min-1。
③在右图中画出第二步反应的平衡常数K随温度的变化的示意图。
查看答案和解析>>
科目:高中化学 来源:2015-2016学年浙江省台州市高一上学期第一次月考化学试卷(解析版) 题型:填空题
用于分离或提纯物质的方法有:A 蒸馏(分馏) B 盐析C 过滤 D 重结晶 E 升华 F 渗析 G 加热分解 。下列各组混合物的分离或提纯应选用上述哪一种方法最合适?(把选用的方法的标号填入括号内)
(1)除去Ca(OH)2溶液中悬浮的CaCO3微粒( )
(2)除去Fe(OH)3胶体中混有的Cl-离子( )
(3)除去乙醇中的少量水( )
(4)除去氧化钙中的碳酸钙( )
(5)除去固体碘中混有的砂子( )
查看答案和解析>>
科目:高中化学 来源:2016届北京市高三上学期期中测试化学试卷(解析版) 题型:选择题
下列解释事实的化学方程式或离子方程式,不正确的是
A.汽车尾气中发生的催化转化反应:2NO+2CO N2+2CO2
N2+2CO2
B.自然界中正常的雨水呈酸性:H2O + CO2  H2CO3
H2CO3 H+ +HCO3-
H+ +HCO3-
C.用CaSO4治理盐碱地:CaSO4(s)+ Na2CO3(aq) CaCO3(s)+ Na2SO4(aq)
CaCO3(s)+ Na2SO4(aq)
D.用FeSO4除去酸性废水中Cr2O72-: Cr2O72- + Fe2+ + 14H+ = 2Cr3+ + Fe3++ 7H2O
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com