
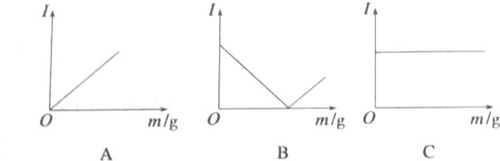
分析 溶液的导电性与离子浓度大小有关,离子浓度越大,溶液导电性越强,结合反应的离子方程式或化学方程式以及电解质的强弱进行判断.
解答 解:A、Ba(OH)2+H2SO4=BaSO4↓+2H2O,滴入H2SO4时,导电性减弱,完全反应后,H2SO4过量,导电性又增强,与B一致;
B、CH3COOH+NH3•H2O=CH3COONH4+H2O,导电性增强,但氨水过量后,将溶液稀释,导电性减弱,与A一致;
C、Ca(OH)2+CO2=CaCO3↓+H2O,导电性减弱,CO2过量后,CaCO3+CO2+H2O?Ca(HCO3)2,Ca(HCO3)2电离使导电性又增强,与B一致;
D、NH4Cl+NaOH=NaCl+NH3•H2O,原为强电解质NH4Cl,反应后仍为强电解质NaCl,NH3•H2O影响不大,与C一致,
E、向饱和的氢硫酸溶液中通入过量的二氧化硫,首先生成单质硫和水,二氧化硫过量与水反应生成亚硫酸电离产生阴、阳离子导电能力增强,与B一致;
故答案为:B;ACE;D.
点评 本题考查酸碱混合及溶液的导电性,明确电解质的强弱、离子浓度与导电性的关系即可解答,题目难度不大.


科目:高中化学 来源: 题型:选择题
| A. | 纯碱、烧碱均属于碱 | |
| B. | CuSO4•5H2O、液氨均属于纯净物 | |
| C. | 凡能电离出H+的化合物均属于酸 | |
| D. | NaCl H2SO4 BaSO4 NH3均属于电解质 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| a | |||
| b | c | d |
| A. | 离子半径:b>c>d>a | |
| B. | bn+与dm-在水溶液中可形成化合物bmdn | |
| C. | 简单氢化物的稳定性:a<c | |
| D. | b和d的最高价氧化物对应的水化物可相互反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 标准状况下,5.6LCO2与足量Na2O2反应转移的电子数为0.5NA | |
| B. | 23g Na与足量H2O反应完全后可生成0.5NA个H2分子 | |
| C. | 2 L0.5mol•L-1硫酸钾溶液中阴离子所带电荷数为NA | |
| D. | 标准状况下,11.2L苯中含有分子的数目为0.5NA |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A | B | C | D |
 |  |  |  |
| 处理污水 | 焚烧废弃塑料 | 推广电动汽车 | 风力发电 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com