
【题目】己知1mol SO2(g)氧化为1mol SO3(g)的能量变化如图所示:反应过程
(1)由图可知该反应为(填“吸热”或“放热”)反应.
(2)该反应通常用V2O5作催化剂,加入V2O5会使图中E1(填“增大”、“减小”或“不变”),加入V2O5 后该反应的△H(填“增大”、“减小”或“不变”).
(3)已知,2H2S(g)+O2(g)═2S(s)+2H2O(g)△H=﹣442.4kJ/mol ①S(s)+O2(g)═SO2(g)△H=﹣297.0kJ/mol ②
H2S(g)与O2(g)反应产生SO2(g)和H2O(g)韵热化学方程式是 .
【答案】
(1)放热
(2)减小;不变
(3)2H2S(g)+3O2(g)═2SO2(g)+2H2O(g)△H=﹣1036.4kJ/mol
【解析】解:(1)根据图示:反应物的能量高于产物,所以反应是放热的;所以答案是:放热;(2)E1为活化能,活化能的大小与反应热无关,加入催化剂能降低反应的活化能,所以答案是:减小;不变;(3)已知2H2S(g)+O2(g)═2S(s)+2H2O(g)△H=﹣442.4kJ/mol ①S(s)+O2(g)═SO2(g)△H=﹣297.0kJ/mol ②①+②×2得到2H2S(g)+3O2(g)═2SO2(g)+2H2O(g),根据盖斯定律,2H2S(g)+3O2(g)═2SO2(g)+2H2O(g)△H=(﹣442.4kJ/mol)+2(﹣297.0kJ/mol)=﹣1036.4kJ/mol.所以答案是:2H2S(g)+3O2(g)═2SO2(g)+2H2O(g)△H=﹣1036.4kJ/mol.
【考点精析】本题主要考查了反应热和焓变的相关知识点,需要掌握在化学反应中放出或吸收的热量,通常叫反应热才能正确解答此题.


科目:高中化学 来源: 题型:
【题目】近年来“雾霾”污染日益严重,原因之一是机动车尾气中含有NO、NO2、CO等气体,减少氮的氧化物在大气中的排放是环境保护的重要内容之一.
(1)已知:N2(g)+O2(g)=2NO(g) △H=+180.5kJmol﹣l
C(s)+O2(g)=CO2(g) △H=﹣393.5kJmol﹣l
2C(s)+O 2(g)=2CO(g) △H=﹣221kJmol﹣l
若某反应的平衡常数表达式为K= ,请写出此反应的热化学方程式__________________________________________________________。
,请写出此反应的热化学方程式__________________________________________________________。
(2)N2O5在一定条件下可发生分解:2N2O5(g)![]() 4NO2(g)+O2(g)。若在恒容绝热的密闭容器中充入一定量 N2O5进行该反应,下列选项能判断该反应达到平衡状态的是_______。
4NO2(g)+O2(g)。若在恒容绝热的密闭容器中充入一定量 N2O5进行该反应,下列选项能判断该反应达到平衡状态的是_______。
A.v 正(N2O5)=2v 逆(NO2) B.容器内NO2浓度是O2浓度的4倍
C.平衡常数K不再随时间而变化 D.混合气体的密度保持不变
E.混合气体的压强不随时间而变化
(3)工业上也可以利用I2O5消除CO的污染。已知:5CO(g)+I2O5(s)![]() 5CO2(g)+I2(s),不同温度下,向装有足量I2O5固体的4L恒容密闭容器中通入2mol CO,测得CO2的体积分数随时间变化的曲线如下图。回答下列问题:
5CO2(g)+I2(s),不同温度下,向装有足量I2O5固体的4L恒容密闭容器中通入2mol CO,测得CO2的体积分数随时间变化的曲线如下图。回答下列问题:

①下列说法正确的是______________
A.d点时,增大体系压强,CO的转化率变大
B.T2时,0~2.0min内的反应速率v(CO)=0.6molL﹣lmin﹣l
C.b点时,向平衡体系中再加入I2O5(s),平衡向正反应方向移动
D.c点时体系中混合气体的压强在T2温度下更大
②5CO(g)+I2O5(s)![]() 5CO2(g)+I2(s)△H=_________0(填“>”、“=“、“<“),判断理由是______________________________________________。
5CO2(g)+I2(s)△H=_________0(填“>”、“=“、“<“),判断理由是______________________________________________。
(4)N2O4与 NO2之间存在反应:N2O4(g)![]() 2NO2(g)△H=QkJmol﹣l.将一定量的 N2O4放入恒容密闭容器中,测得其平衡转化率[α(N2O4)]随温度变化如下图所示.如图 中 a 点对应温度下,已知 N2O4的起始压强 p0为 200kPa,该温度下反应的平衡常数的计算表达式Kp=______________(用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)。
2NO2(g)△H=QkJmol﹣l.将一定量的 N2O4放入恒容密闭容器中,测得其平衡转化率[α(N2O4)]随温度变化如下图所示.如图 中 a 点对应温度下,已知 N2O4的起始压强 p0为 200kPa,该温度下反应的平衡常数的计算表达式Kp=______________(用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列叙述中,你认为科学的是( )
A. 某广告语:本饮料纯属天然物质,不含任何化学成分
B. 到城乡结合处燃放鞭炮,可避免污染环境
C. 在地球上分布很广,淡水资源取之不尽,用之不竭
D. 大气中二氧化碳含量的增多是造成“温室效应”的主要原因
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图立方烷(C8H8)的球棍模型,下列有关说法不正确的是( ) 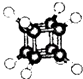
A.它的一氯代物只有一种同分异构体
B.它的二氯代物有三种同分异构体
C.它与苯乙烯(C6H5﹣CH=CH2)互为同分异构体
D.它是一种不饱和烃,既能发生取代反应,又能发生加成反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是
A.“冰水混合物”是一种分散系B.水溶液中能电离出H+的化合物一定是酸
C.盐中一定含有金属元素D.在氧化还原反应中,金属单质作为反应物只能做还原剂
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】研究人员研制出一种可快速充放电的超性能铝离子电池,Al、Cn为电极,有机阳离子与阴离子(AlCl![]() 、Al2Cl
、Al2Cl![]() )组成的离子液体为电解质。如图为该电池放电过程示意图。下列说法错误的是( )
)组成的离子液体为电解质。如图为该电池放电过程示意图。下列说法错误的是( )
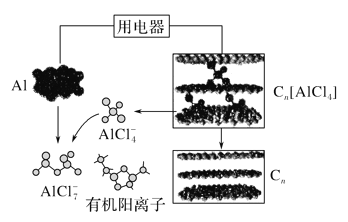
A. 充电时,Al做阴极、Cn为阳极
B. 充电时,每生成1 mol铝,同时消耗4 mol Al2Cl![]()
C. 放电时,电解质中的有机阳离子向铝电极方向移动
D. 放电时,正极反应式为Cn[AlCl4]+ e-=== Cn + AlCl![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】按要求完成下列式子:
(1)S2-离子结构示意图____________,CO2的电子式__________________,NH3的结构式_________________。
(2)写出磁铁矿的化学式______________。
(3)写出一水合氨(NH3·H2O)在水中的电离方程式______________。
(4)写出实验室制取氯气的离子方程式____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于Fe(OH)3胶体的说法中,不正确的是
A. 分散质粒子直径在l0-9~10-7m之间 B. 是一种纯净物
C. 具有丁达尔效应 D. 具有净水作用
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com