
请回答下面问题:
(1)甲同学想通过实验测得的数据是_________。他使用装置③_______(填“有”或“没有”)必要。
(2)乙同学想通过实验测得的数据是_________。按他测得的数据计算出的实验结果_________。(填“偏高”或“偏低”),理由是____________________________________________。
(3)为了测得准确的实验数据,请你将乙同学的实验装置进行改进(每种仪器只准使用一次),写出各仪器接口的连接顺序:___________________________。
(4)按你设计的实验装置进行实验,若测得实验前后装置②的质量分别是W1和W2,则样品中过碳酸钠的质量分数为_________。
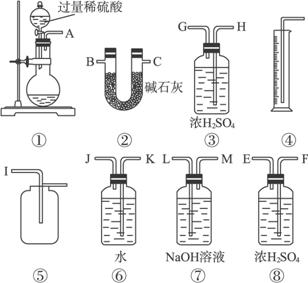
解析:(1)⑦中NaOH吸收了CO2,⑥④是测气体体积的装置,所以测量的是O2的体积,由于采用排水法测体积,所以干燥是没必要的。
(2)碱石灰吸取CO2,同时也吸水气,所以乙测的是CO2的质量(常温下水是液态),其结果偏高。
(3)在②前加干燥装置除去水气,在②后加干燥装置防止空气中水、CO2干扰。
(4)m(CO2)=W2-W1,n(Na2CO4)=n(CO2)=![]() (mol)
(mol)
m(Na2CO4)=122![]() (g)
(g)
ω=![]() ×100%=
×100%=![]()
答案:(1)氧气的体积 没有
(2)二氧化碳的质量 偏高 气体中的水蒸气被碱石灰吸收,同时空气中的二氧化碳和水蒸气也被碱石灰吸收
(3)AHGBCFE或AFEBCHG(B、C可交换)
(4)![]()


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com