
ͼ������ʵ���ҽ��а��������Ʊ�������ʵ������װ�ã����̶ֹ�װ��δ������
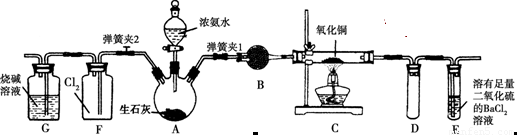
��1������װ��װ�ú���Ҫ����A��Eװ�õ������ԣ������������___???????? _____����E��װ��ˮ��Ȼ����A���۲쵽E��������ð�����ƿ��ƾ��ƻ��ɿ�˫�֣�E�е�����ˮ���γɣ�˵��װ�����������á�
��2��װ��B��ʢ�ŵ��Լ���________��
��3����ȼC���ƾ��ƣ��رյ��ɼ�2�����ɼ�1���ӷ�Һ©���ų�Ũ��ˮ����û��ƿ�й����رշ�Һ©�����Ժ�Ƭ�̣�װ��C�к�ɫ������죬װ��E����Һ����ִ������ݣ�ͬʱ����________(������)����E���ݳ�Һ����������ֱ�������������д����C�з�����Ӧ�Ļ�ѧ����ʽ��________________________��
��4���ڹرյ��ɼ�1���ɼ�2�������������F�У��ܿ췢��װ��F�в������̣�ͬʱ����G����ҺѸ�ٵ�������F�У�д���������̵Ļ�ѧ����ʽ��____________________��Ѹ�ٲ���������ԭ����____________________________��
��1���رյ��ɼ�2�ͷ�Һ©�����������ɼ�1(2��)
��2����ʯ��(����ʯ��) (2��)
��3����ɫ����(2��)��?????? 2NH3��3CuO 3Cu��N2����3H2O(2��)
3Cu��N2����3H2O(2��)
��4��3Cl2��8NH3=N2��6NH4Cl(2��)
ʢ�������ļ���ƿ�����������������ɲ��ֹ��壬ƿ��ѹǿ��С����Һ����(2��)
��������
�����������1�����װ�õ������Ե���Ҫǰ�����γɷ�յ���ϵ������Ҫ�ȹرյ��ɼ�2�ͷ�Һ©�����������ɼУ���2��B�Ǹ���NH3��װ�ã�����NH3��ʹ�ü��Ը����������ʹ�ü�ʯ�ң���3�� C��CuO��NH3����������ԭ��Ӧ���ɺ�ɫ��Cu��N2��H2O ������Ӧ�ķ���ʽΪ��2NH3��3CuO 3Cu��N2����3H2O��E�Ǵ���NH3��β��װ�ã�E�з�����Ӧ��2NH3��BaCl2��SO2��H2O=BaSO3����2NH4Cl�����������Dz�����ɫ������ ��4�� �رյ��ɼ�1���ɼ�2��Cl2�ɽ�NH3����ΪN2��ͬʱ���ɵ�HCl���NH3��Ӧ����NH4Cl��������������Fƿ��ѹǿ��С�Ӷ����ֵ�������
3Cu��N2����3H2O��E�Ǵ���NH3��β��װ�ã�E�з�����Ӧ��2NH3��BaCl2��SO2��H2O=BaSO3����2NH4Cl�����������Dz�����ɫ������ ��4�� �رյ��ɼ�1���ɼ�2��Cl2�ɽ�NH3����ΪN2��ͬʱ���ɵ�HCl���NH3��Ӧ����NH4Cl��������������Fƿ��ѹǿ��С�Ӷ����ֵ�������
���㣺���鰱�����Ʊ������������ʡ������Լ���֪ʶ��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�





| ���� |
| �� |
| ���� |
| �� |


| ����� |
 +14CD2T2����ͬ�������£�������з�Ӧ��2CH3CH2OD+C18O2
+14CD2T2����ͬ�������£�������з�Ӧ��2CH3CH2OD+C18O2| ����� |


�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�


| ||
| �� |
| ||
| �� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ��Ķ�����
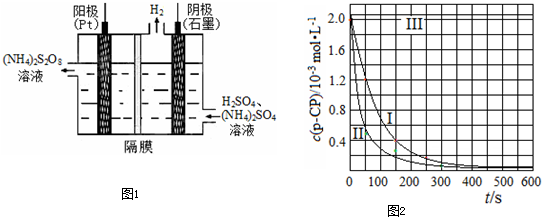
 ��2013?������һģ���£�N2H4���Ͱ��ǵ������ֳ���������ڿ�ѧ�������������й㷺Ӧ�ã��밴Ҫ��ش��������⣺
��2013?������һģ���£�N2H4���Ͱ��ǵ������ֳ���������ڿ�ѧ�������������й㷺Ӧ�ã��밴Ҫ��ش��������⣺

| ||
| ||
| T/�� | 165 | 175 | 185 | 195 |
| K | 111.9 | 74.1 | 50.6 | 34.8 |
| n(NH3) |
| n(CO2) |
| n��N2�� | n��H2�� | n��NH3�� | |
| �� | 1mol | 3mol | 0mol |
| �� | 0.5mol | 1.5mol | 1mol |
| �� | 0mol | 0mol | 4mol |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ��Ķ�����
| 1 |
| x |
| 1 |
| x |
| 3 |
| x |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| ʵ�� ��� |
T/K | pH | c/10-3mol?L-1 | |
| H2O2 | Fe2+ | |||
| �� | 298 | 3 | 6.0 | 0.30 |
| �� | 313 | 3 | 6.0 | 0.30 |
| �� | 298 | 10 | 6.0 | 0.30 |
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com