
可逆反应:2NO2  2NO+O2在体积固定的密闭容器中,达到平衡状态的标志是( )
2NO+O2在体积固定的密闭容器中,达到平衡状态的标志是( )
①单位时间内生成n mol O2的同时生成2n mol NO2
②单位时间内生成n mol O2的同时生成2n mol NO
③用NO2、NO、O2的物质的量浓度变化表示的反应速率的比为2∶2∶1的状态
④混合气体的颜色不再改变的状态
⑤混合气体的密度不再改变的状态
⑥混合气体的压强不再改变的状态
⑦混合气体的平均相对分子质量不再改变的状态
A.①④⑥⑦ B.②③⑤⑦ C.①③④⑤ D.全部
A
【解析】
试题分析:①单位时间内生成n mol O2的同时生成2n mol NO2代表正逆反应的速率且满足化学方程式中的系数比,符合正逆反应速率相等,可以判断平衡的到达,正确;②单位时间内生成n mol O2的同时生成2n mol NO代表的都是正反应方向,不能判断平衡的到达,错误;③用NO2、NO、O2的物质的量浓度变化表示的反应速率的比为2∶2∶1的状态不一定是平衡状态,错误;④体积固定时,混合气体的颜色逐渐变浅,达平衡时颜色不再变化,所以混合气体的颜色不再改变的状态是平衡状态,正确;⑤体积固定时,混合气体的密度一直不变,不能作为平衡到达的标志,错误;⑥体积固定时,混合气体的压强一直增大,达平衡时不再变化,所以混合气体的压强不再改变的状态是平衡状态,正确;⑦该反应是气体的物质的量发生改变的可逆反应,所以混合气体的平均相对分子质量一直在变化,达平衡时不再变化,所以混合气体的平均相对分子质量不再改变的状态是平衡状态,正确,所以答案选A。
考点:考查化学平衡的标志的判断


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源:2013-2014江西省九江七校下学期期中联考高二化学试卷(解析版) 题型:选择题
已知乙炔(C2H2)、苯(C6H6)、乙醛(C2H4O)的混合气体中含氧元素的质量分数为8%,则混合气体中碳元素的质量分数为( )
A.84% B.60% C.91% D.42%
查看答案和解析>>
科目:高中化学 来源:2013-2014江西省高二下学期期末考试化学试卷(解析版) 题型:选择题
组成和结构可用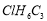
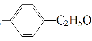 表示的有机物中,能发生消去反应的共有( )
表示的有机物中,能发生消去反应的共有( )
A.10种 B.16种 C.20种 D.25种
查看答案和解析>>
科目:高中化学 来源:2013-2014江西省高一下学期期末考试化学试卷(解析版) 题型:填空题
(10分) A、B、C、D、E是位于短周期的主族元素。已知:①热稳定性:HmD>HmC;②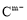 、
、 具有相同的电子层结构;③A与B在同一周期,在该周期所有主族元素中,A的原子半径最大,B的离子半径最小;④A与B质子数之和是D质子数的3倍。依据上述信息用相应的化学用语回答下列问题:
具有相同的电子层结构;③A与B在同一周期,在该周期所有主族元素中,A的原子半径最大,B的离子半径最小;④A与B质子数之和是D质子数的3倍。依据上述信息用相应的化学用语回答下列问题:
HmDm的电子式___________________。(1分)
能证明 、
、 的还原性强弱的离子方程式为__________________________________。
的还原性强弱的离子方程式为__________________________________。
(3)将E的单质通入A与D形成的化合物的水溶液中,其离子方程式为:__________________________。
(4)常温下,将等物质的量浓度的HmC溶液和A的最高价氧化物对应的水化物溶液等体积混合,写出该反应的离子方程式 。
在该溶液中溶质中含有的化学键类型是 (1分)
(5)在A、B、C、E单质中,符合下列转化关系的是_____________(填元素符号)。

查看答案和解析>>
科目:高中化学 来源:2013-2014江西省高一下学期期末考试化学试卷(解析版) 题型:选择题
燃料电池是燃料(如H2、CO、CH4等)跟氧气或空气起反应,将化学能转变为电能的装置,电解液为强碱溶液。下列关于甲烷燃料电池的说法正确的是( )
A.负极反应为CH4+10OH-→CO32-+7H2O+8e-
B.负极反应为O2+2H2O+4e-→4OH-
C.随着放电进行,溶液中的阳离子向负极移动
D.随着放电进行,溶液的PH不变
查看答案和解析>>
科目:高中化学 来源:2013-2014江西省高一下学期期末考试化学试卷(解析版) 题型:选择题
下列说法正确的是( )
A.原子最外层只有1个电子的元素一定是金属元素
B.原子最外层只有2个电子的元素一定是金属元素
C.最外层电子数比次外层电子数多的元素一定位于第二周期
D.某元素的离子最外层电子数与次外层电子数相同,该元素一定位于第三周期
查看答案和解析>>
科目:高中化学 来源:2013-2014江西省上饶市高三六校第二次联考理综化学试卷(解析版) 题型:填空题
(14分)运用化学反应原理分析解答以下问题
(1)已知: ①CO(g)+2H2(g)  CH3OH(g) △Hl= -91kJ·mol-l
CH3OH(g) △Hl= -91kJ·mol-l
②2CH3OH(g) CH3OCH3(g)+H2O(g) △H2= -24 kJ·mol-l ③CO(g) +H2O(g)
CH3OCH3(g)+H2O(g) △H2= -24 kJ·mol-l ③CO(g) +H2O(g)  CO2(g)+H2(g) △H3= -41 kJ·mol-l
CO2(g)+H2(g) △H3= -41 kJ·mol-l
且三个反应的平衡常数依次为K1、K2、K3
 则反应 3CO(g) +3H2(g) CH3OCH3(g) +CO2(g) △H= .
则反应 3CO(g) +3H2(g) CH3OCH3(g) +CO2(g) △H= .
化学平衡常数K= (用含K1、K2、K3的代数式表示)。
(2)一定条件下,若将体积比为1:2的CO和H2气体通入体积一定的密闭容器中发生反应
 3CO(g) +3H2(g) CH3OCH3(g) +CO2(g),下列能说明反应达到平衡状态是 。
3CO(g) +3H2(g) CH3OCH3(g) +CO2(g),下列能说明反应达到平衡状态是 。
a.体系压强保持不变 B.混合气体密度保持不变
c. CO和H2的物质的量保持不变 d.CO的消耗速度等于CO2的生成速率
(3)氨气溶于水得到氨水。在25℃下,将x mol.L-l的氨水与y mol.L-1的盐酸等体积混合,反应后溶液显中性,则c(NH4+)____c(Cl-)(填“>”、“<”、“=”);用含x和y的代数式表示出氨水的电离平衡常数 .
(4)科学家发明了使NH3直接用于燃料电池的方法,其装置用铂黑作电极、加入电解质溶液中,一个电极通入空气,另一电极通入NH3。其电池反应式为:4NH3+3O2 = 2N2+6H2O,电解质溶液应显 (填“酸性”、“中性”、“碱性”),
写出正极的电极反应方程式 .
查看答案和解析>>
科目:高中化学 来源:2013-2014江西省上饶市第二学期期末教学质量测试高二化学试卷(解析版) 题型:选择题
香叶醇是合成玫瑰香油的主要原料,其结构简式如下,
?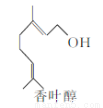
下列有关香叶醇的叙述正确的是
A.香叶醇的分子式为C10H18O
B.不能使溴的四氯化碳溶液褪色
C.不能使酸性高锰酸钾溶液褪色
D.能发生加成反应不能发生取代反应
查看答案和解析>>
科目:高中化学 来源:2013-2014江苏省盐城市高二下学期期终考试化学试卷(解析版) 题型:填空题
(12分)今有氧、镁、铝、硫、铬5种元素,试回答下列问题
(1)镁晶体堆积方式为 堆积(选填:“简单立方”、“体心立方”、“面心立方”、“六方”);
(2)用“>”、“<”填写下表
第一电离能 | 电负性 | 晶格能 | 沸点 |
Mg Al | O S | MgO MgS | H2O H2S |
(3)基态铬原子外围电子轨道表示式为 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com