
【题目】【化学—选修5有机化学基础】邻苯二甲酸二乙酯![]() 是一种重要的工业塑化剂,其合成路线很多,下图就是其中的一种合成方法:
是一种重要的工业塑化剂,其合成路线很多,下图就是其中的一种合成方法:

已知以下信息:
① 有机化合物A可用来催熟水果。
② 有机化合物C的核磁共振氢谱显示其有3种不同化学环境的氢原子。

(1)A的化学名称是 ,B的结构简式为 。
(2)反应Ⅱ的试剂是 ,该反应类型为 。
(3)C生成D的化学方程式为 。
(4)E生成F的化学方程式为 。
(5)在G的同分异构体中,既能与新制的Cu(OH)2悬浊液在加热条件下反应生成砖红色沉淀,又能与碳酸钠反应生成二氧化碳,还能使FeCl3溶液显色的有 种,所有这些同分异构体中,不同化学环境氢原子的种数 (填“相同”“不相同”)。
【答案】(1)乙烯;CH3CH2OH;(2)强碱的水溶液;取代反应或水解反应
(3)![]()
![]()
![]()
![]()
(4)![]()
(5)10;相同
【解析】
试题分析:由邻苯二甲酸二乙酯结构可以知道,邻苯二甲酸和乙醇发生酯化反应生成,有机化合物A可用来催熟水果,A为CH2=CH2,CH2=CH2中含有不饱和的C=C双键,能够在催化剂存在条件下与水发生加成反应生成B为CH3CH2OH;
G为邻苯二甲酸![]() ,含几种位置的H原子,则核磁共振氢谱就有几种,有机化合物C化学式为C8H10,核磁共振氢谱显示有3种不同化学环境的氢原子,说明含有3种氢原子,则C为
,含几种位置的H原子,则核磁共振氢谱就有几种,有机化合物C化学式为C8H10,核磁共振氢谱显示有3种不同化学环境的氢原子,说明含有3种氢原子,则C为![]() ,与氯气发生取代反应生成D为
,与氯气发生取代反应生成D为![]() ,F能发生银镜反应,说明F为醛,且G为邻苯二甲酸,所以F
,F能发生银镜反应,说明F为醛,且G为邻苯二甲酸,所以F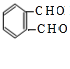 ,则E→F为醇的催化氧化,所以E为
,则E→F为醇的催化氧化,所以E为![]() ,D→E为卤代烃的取代反应,
,D→E为卤代烃的取代反应,
(1)A的化学名称是乙烯,B为乙醇,结构简式为CH3CH2OH,因此,本题正确答案是:乙烯;CH3CH2OH;
(2)反应II为卤代烃的水解反应,其反应条件是强碱的水溶液、加热,所以所用试剂是强碱水溶液,该反应为取代反应或水解反应,因此,本题正确答案是:强碱的水溶液;取代(或水解);
(3)有机化合物C化学式为C8H10,核磁共振氢谱显示有3种不同化学环境的氢原子,说明含有3种氢原子,则C为![]() ,与氯气发生取代反应
,与氯气发生取代反应![]()
![]()
![]()
![]() ,因此,本题正确答案是:
,因此,本题正确答案是:![]()
![]()
![]()
![]() ;
;
(4)E生成F为醇的催化氧化,反应方程式为![]() ,因此,本题正确答案是:
,因此,本题正确答案是:![]() ;
;
(5)G为邻苯二甲酸![]() ,满足下列条件的同分异构体:
,满足下列条件的同分异构体:
能与新制的Cu(OH)2悬浊液混合加热生成砖红色沉淀,含有醛基,又能与碳酸钠反应生成二氧化碳,含有羧基,能与FeCl3溶液发生显色反应,含有酚羟基;说明苯环上有-OH、-CHO、-COOH三个取代基,-OH、-CHO处于邻位,-COOH有4种位置,-OH、-CHO处于间位,-COOH有4种位置,-OH、-CHO处于对位,-COOH有2种位置,有10种;所有这些同分异构体中,不同化学环境氢原子的种数都为6种,因此,本题正确答案是:10;相同.


 期末集结号系列答案
期末集结号系列答案科目:高中化学 来源: 题型:
【题目】如图为二氧化锰的有关转化关系图,有关说法中不正确的是( )
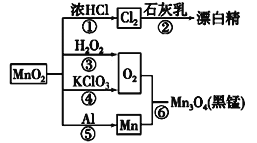
A.反应①~⑥均属于氧化还原反应
B.反应①中氧化剂与还原剂的物质的量之比为1∶4
C.相同条件下生成等量的O2,反应③和④转移的电子数之比为1∶2
D.反应②中Cl2既是氧化剂又是还原剂
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一定温度下,固定体积为2L密闭容器中,发生反应:
2SO2(g)+O2(g)![]() 2SO3(g ) ΔH <0,n(SO2)随时间的变化如表:
2SO3(g ) ΔH <0,n(SO2)随时间的变化如表:
时间/min | 0 | 1 | 2 | 3 | 4 | 5 |
n(SO2)/mol | 0.20 | 0.16 | 0.13 | 0.11 | 0.08 | 0.08 |
则下列说法正确的是
A. 当v(SO2)=v(SO3)时,说明该反应已达到平衡状态
B. 用O2表示0~4 min内该反应的平均速率为0.005 mol/(L·min)
C. 平衡时再通入O2,平衡右移,O2转化率减小,SO2转化率增大
D. 若升高温度,则SO2的反应速率会变大,平衡常数K值会增大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】加热条件下浓硫酸能将木炭粉氧化成CO2,本身被还原成SO2。试用如图所列各装置设计一个实验,来验证上述反应所产生的各种产物。
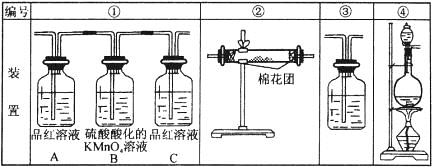
(1)这些装置的连接顺序是(按产物气流从左至右的方向,填写装置的编号):______→____→____→____。
(2)实验时可观察到装置①中A瓶的溶液褪色。A瓶溶液的作用是_________,B瓶溶液的作用是_______, C瓶溶液的作用是________________。写出B中发生的离子方程式__________。
(3)装置②中所加的固体药品是____________,可验证的产物是____________。
(4)装置③中所盛溶液是_____________,可验证的产物是__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】聚合硫酸铁又称聚铁,化学式为[Fe2(OH)n(SO4)3-0.5n]m,广泛用于污水处理。实验室利用硫酸厂烧渣(主要成分为铁的氧化物及少量FeS、SiO2等)制备聚铁和绿矾(FeSO4·7H2O),过程如下:

(1)验证固体W焙烧后产生的气体含有SO2的方法是 。
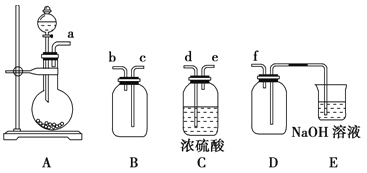
(2)实验室制备、收集干燥的SO2,所需仪器如下。装置A产生SO2,写出实验室制备SO2气体化学方程式: 按气流方向连接各仪器接口,顺序为a→ → → → →f。装置D的作用是 。
(3)制备绿矾时,向溶液X中加入过量 ,充分反应后,经 操作得到溶液Y,再经浓缩、结晶等步骤得到绿矾。
(4)溶液Z的pH影响聚铁中铁的质量分数,用pH试纸测定溶液pH,下列记录结果正确的是:( )
a. 氯水的PH为2.3 b. 氢氧化钠溶液的PH为11.0
c. 硫酸铁溶液的PH为1 d. 硫酸氢钠溶液的PH为7
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】市场上经常见到的标记为Li-ion的电池称为“锂离子电池”。它的负极材料是金属锂和碳的复合材料(碳作为金属锂的载体),电解质为一种能传导Li+的高分子材料。这种锂离子电池的电池反应式为:Li+2Li0.35NiO2![]() 2Li0.85NiO2,下列说法不正确的是( )
2Li0.85NiO2,下列说法不正确的是( )
A.放电时,负极的电极反应式:Li-e-===Li+
B.充电时,Li0.85NiO2既发生氧化反应又发生还原反应
C.该电池不能用水溶液作为电解质溶液
D.放电过程中Li+向负极移动
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某酸性溶液中只有Na+、CH3COO﹣、H+、OH﹣四种离子.则下列描述正确的是
A.该溶液可由pH=3的CH3COOH与pH=11的NaOH溶液等体积混合而成
B.该溶液可由等物质的量浓度、等体积的NaOH溶液和CH3COOH溶液混合而成
C.加入适量NaOH,溶液中离子浓度为c(CH3COO﹣)>c(Na+ )>c(OH﹣)>c(H+)
D.加入适量氨水,c(CH3COO﹣)一定大于c(Na+)、c(NH4+)之和
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列科学成果中,由我国化学家在现代化学研究中取得的是( )
A.发现放射性元素钋和镭
B.现代量子化学的创立
C.人工全合成牛胰岛素
D.元素周期律的发现
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是 ( )
A. 酸碱中和反应是吸热反应
B. 吸热反应不加热就不会发生
C. 放热反应不用加热也一定能发生
D. 反应是放热还是吸热可以看反应物和生成物所具有的总能量的相对大小
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com