
| 溶质 | CH3COONa | NaHCO3 | Na2CO3 | NaClO | NaCN |
| pH | 8.8 | 9.7 | 11.6 | 10.3 | 11.1 |
| 离子 | Fe2+ | Cu2+ | Mg2+ |
| pH | 7.6 | 5.2 | 10.4 |
分析 (1)越容易水解的盐,越容易结合氢离子,相同浓度的钠盐溶液,pH越大则盐的水解程度越大,浓度相同的酸稀释相同的倍数后,酸性越强的酸其pH变化越大;
(2)碳酸钠和碳酸氢钠促进水的电离,水解程度大,则水的电离程度大;Na2CO3溶液中CO32-的水解大于碳酸氢钠中HCO3-的水解,据此进行判断;
(3)①根据盐类的水解和电荷守恒来分析,注意盐类的水解是微弱的;
②开始沉淀时pH小的离子先沉淀,溶度积常数越小的物质越先沉淀;0.2mol/L的CuSO4溶液中Cu2+沉淀较为完全(使Cu2+浓度降至原来的千分之一)则应向溶液里加NaOH溶液,c(Cu2+)=0.0002mol/L,根据Ksp计算pH.
解答 解:(1)越容易水解的盐,越容易结合氢离子,相同浓度的钠盐溶液,pH越大则盐的水解程度越大,所以最易水解的盐是碳酸钠,所以最容易结合氢离子的阴离子是CO32-;浓度相同的酸稀释相同的倍数后,酸性越强的酸其pH变化越大,HCN、HClO、CH3COOH、H2CO3四种酸的酸性大小顺序是CH3COOH>H2CO3>HClO>HCN,所以溶液的pH变化最大的是醋酸,故选C,
故答案为:CO32-;C;
(2)碳酸钠和碳酸氢钠促进水的电离,碳酸根离子水解程度大,则碳酸钠中水的电离程度大,即溶液中水电离出的H+个数:②>①,Na2CO3溶液中CO32-的水解大于乙中HCO3-的水解,则碳酸钠中阴离子浓度之和大,即溶液中阴离子的物质的量浓度之和:②>①,
故答案为:<;<;
(3)①300mL 1mol•L-1的NaOH的物质的量=1mol/L×0.3L=0.3mol,标准状况下4.48LCO2的物质的量=$\frac{4.48L}{22.4L/mol}$=0.2mol,所以氢氧化钠和二氧化碳反应方程式为2CO2+3NaOH=Na2CO3+NaHCO3+H2O,溶液中碳酸根离子水解而使溶液呈碱性,即c(OH-)>c(H+),碳酸根离子水解生成碳酸氢根离子,所以c(HCO3-)>c(CO32-),由于水解程度较小,所以c(CO32-)>c(OH-),故溶液中各离子浓度大小顺序是c(Na+)>c(HCO3-)>c(CO32-)>c(OH-)>c(H+),
故答案为:c(Na+)>c(HCO3-)>c(CO32-)>c(OH-)>c(H+);
②pH小的离子先沉淀,溶度积常数越小的物质越先沉淀,所以Cu2+先沉淀,KSP[(Fe(OH)2]<KSP[(Mg(OH)2],0.2mol/L的CuSO4溶液中Cu2+沉淀较为完全(使Cu2+浓度降至原来的千分之一)则应向溶液里加NaOH溶液,c(Cu2+)=0.0002mol/L,c(OH-)=$\sqrt{\frac{2×1{0}^{-20}}{2×1{0}^{-4}}}$=10-8mol/L,c(H+)=10-6mol/L,所以pH=6,
故答案为:Cu2+;<;6.
点评 本题考查了弱电解质的电离、盐的水解、离子浓度的比较、Ksp的应用等知识点,题目考查的知识点较多,题目难度中等,注意把握溶液中离子浓度大小比较的方法.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:选择题
| A. | 1 mol NH4+ 所含质子数为10NA | |
| B. | 10克氖气所含原子数约为6.02×1023 | |
| C. | 常温常压下,22.4 L SO2所含的分子数为NA | |
| D. | 常温常压下,32 g O2和O3的混合气体所含原子数为2NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 点燃爆竹后,硫燃烧生成SO3 | |
| B. | 中国古代利用明矾溶液的酸性清除铜镜表面的铜锈 | |
| C. | 服用阿司匹林出现水杨酸反应时,用NaHCO3溶液解毒 | |
| D. | 高铁车厢大部分材料采用铝合金,因为铝合金强度大、质量轻、抗腐蚀能力强 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用氨水清洗试管内壁附着的银镜 | |
| B. | 将NH4Cl溶液蒸干制备NH4Cl固体 | |
| C. | 鉴别氯化钠溶液、氢氧化钠溶液和稀盐酸,各取少量溶液于试管中,分别滴加紫色石蕊溶液,观察溶液颜色的变化 | |
| D. | 制备Fe(OH)3胶体,向盛有沸水的烧杯中滴加FeCl3饱和溶液并长时间煮沸 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
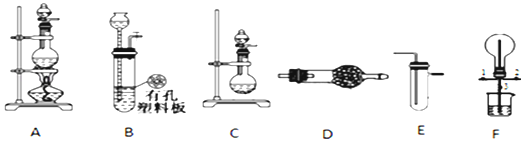
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 0.5L 2mol/LBaCl2溶液中,钡离子和氯离子总数约为3NA | |
| B. | 从1L 1mol/L的NaCl溶液中取出10mL,其浓度仍为1mol/L | |
| C. | 配置0.5L 10mol/L的盐酸,需要标准状况下的氯化氢气体112L | |
| D. | 10mL质量分数为98%的硫酸,用水稀释至100mL,硫酸的质量分数为9.8% |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com