
常温下,用Na2SO3溶液吸收SO2时,溶液pH随n(SO32-):n(HSO3-)变化的关系如下表:
|
n(SO32-):n(HSO3-) |
91:1 |
1:1 |
9:91 |
|
pH |
8.2 |
7.2 |
6.2 |
以下离子浓度关系的判断正确的是
A.NaHSO3溶液中c(H+)<c(OH-)
B.Na2SO3溶液中c(Na+)>c(SO32-)>c(HSO3-)>c(OH-)>c(H+)
C.当吸收液呈中性时,c(Na+)>c(SO32-)>c(HSO3-)>c(OH-)=c(H+)
D.当吸收液呈中性时,c(Na+)= c(HSO3-)+2 c(SO32-)
D
【解析】
试题分析:A、用Na2SO3溶液吸收SO2时,随着吸收的增多,溶液由碱性逐渐变为酸性。由表中信息可知NaHSO3溶液为酸性溶液,因此c(H+)>c(OH-),A项错误;
B、Na2SO3溶液中SO32-的水解分两步进行,且以第一步水解为主,所以c (HSO3-)应小于c (OH-),故B项错误;
C、由表中数据,当c (SO32-)=c (HSO3-)时,pH=7.2,因此当吸收液呈中性时,可推出c (SO32-)<c (HSO3-) ,所以C项错误;
D、溶液显中性,则c(H+)=c (OH-),根据电荷守恒c(Na+)+c(H+)=c(OH-)+c(HSO3-)+2 c(SO32-),所以c(Na+)=c (HSO3-)+2c (SO32-),D正确,答案选D。
考点:考查溶液中离子浓度大小比较以及溶液酸碱性的判断等


 阶梯计算系列答案
阶梯计算系列答案科目:高中化学 来源: 题型:阅读理解
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
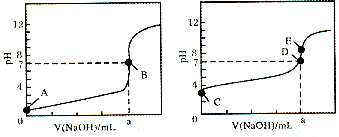
(2013?日照一模)常温下,用Na2SO3溶液吸收SO2时,溶液pH随n(
|
查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解
①及时转移疏散人群,同时向有关部门如实报告事故有关情况;②被转移人群应戴上用浓NaOH溶液处理过的口罩;③用高压水枪向空中喷洒含碱性物质的水溶液;④被转移人群可戴上用Na2CO3溶液处理过的口罩(湿润);⑤将人群转移到地势较低的地方即可,不必走太远;⑥及时清理现场,检查水源和食物等是否被污染;⑦常温下氯气能溶于水,所以只要向空气中喷洒水就可以解毒。
据报道,为防止罐中液氯再次泄漏,4月1日抢救人员将盛液氯的罐吊到事故发生地附近刚挖好的水塘中,用烧碱溶液处理。写出反应的离子方程式____________________________。
(2)用氯气对饮用水消毒已有百年历史。这种消毒方法会使饮用水中的有机物发生氯代,生成含氯的有机化合物,对人体有害,世界环保联盟即将全面禁止用氯气对饮用水消毒,建议推广采用广谱高效消毒剂二氧化氯(ClO2)。
我国最近研究成功了用氯气氧化亚氯酸钠(在氮气保护下)制得ClO2,表示这一反应的化学方程式是______________,在H2SO4的酸性条件下,用Na2SO3还原NaClO3也可制得ClO2,在以上反应中NaClO3和Na2SO3的物质的量之比为_______。
(3)一化学课外活动小组的同学制作了一种家用环保型消毒液发生器(如图1-3-3),用石墨作电极电解饱和氯化钠溶液,可制得少量消毒剂。为了研究各电极的产物,反应开始后沿玻璃管滴几滴酚酞试液到溶液中,发现上层溶液变红,一段时间后,红色消失。则与电源a端相连的电极上发生的电极反应式为____________________。

图1-3-3
该小组同学经查阅资料后认为褪色的原因可能有两个:一是氢氧化钠浓度过大;二是。小华设计了一个简单的实验,只需要一种试剂,便获得了有关褪色原因的结论,请简要写出小华设计的实验方案:______________________________________________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com