
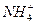 、Na+等离子的七种溶液一次性鉴别开来的试剂是( )
、Na+等离子的七种溶液一次性鉴别开来的试剂是( )| A.NaHCO3溶液 |
| B.KSCN溶液 |
| C.NaOH溶液 |
| D.NH3·H2O溶液 |
 各地期末复习特训卷系列答案
各地期末复习特训卷系列答案 小博士期末闯关100分系列答案
小博士期末闯关100分系列答案科目:高中化学 来源:不详 题型:单选题
| A.必须预估待测液可能的浓度范围,以便配制标准色阶 |
| B.比色法只能粗略测量溶液浓度,不如滴定法精确 |
| C.目视比色要求待测物有灵敏的显色反应 |
| D.配制色阶越多,色阶浓度差越小,比色测定的结果就越精确 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.①②③④ | B.③①②④ | C.④③②① | D.③②①④ |
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
| A.萃取分液 | B.升华 | C.结晶 | D.分液 E.蒸馏 F.过滤 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题

查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.③④ | B.②③④ | C.①②③④ | D.①④ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com