
| A. | Na+、K+、OH-、Cl- | B. | Na+、Cu2+、SO42-、NO3- | ||
| C. | Mg2+、Na+、SO42-、Cl- | D. | Ca2+、HCO3-、NO3-、K+ |
科目:高中化学 来源: 题型:选择题
| A. | 0.1 mol•L-1 CH3COONa溶液与0.1 mol•L-1 HCl溶液等体积混合:c(Na+)=c(Cl-)>c(CH3COO-)>c(OH-) | |
| B. | 0.1 mol•L-1 NH4Cl溶液与0.1 mol•L-1氨水等体积混合(pH>7):c(NH3•H2O)>c(NH4+)>c(Cl-)>c(OH-) | |
| C. | 0.1 mol•L-1 Na2CO3溶液与0.1 mol•L-1 NaHCO3溶液等体积混合:$\frac{3}{2}$c(Na+)=c(CO32-)+c(HCO3-)+c(H2CO3) | |
| D. | 0.1 mol•L-1 Na2C2O4溶液与0.1 mol•L-1 HCl溶液等体积混合(H2C2O4为二元弱酸):2c(C2O42-)+c(HC2O4-)+c(OH-)=c(Na+)+c(H+) |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 ;
;查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 一定条件下,乙酸乙酯、葡萄糖、蛋白质都能与水发生水解反应 | |
| B. | CCl4分子的比例模型为  其空间构型为正四面体 其空间构型为正四面体 | |
| C. | 全降解塑料  可由环氧丙烷 可由环氧丙烷  和CO2缩聚制得 和CO2缩聚制得 | |
| D. | 一定条件下,完全燃烧14g含氧质量分数为a的乙烯、乙醛混合气体,生成水的质量为18(1-a)g |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
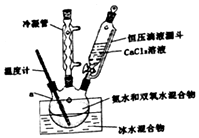 过氧化钙(CaO2)是一种白色结晶体粉末,极微溶于水,不溶于醇类、乙醚等,加热至150℃左右开始分解放出氧气,与水缓慢反应生成H2O2.易于酸反应生成H2O2
过氧化钙(CaO2)是一种白色结晶体粉末,极微溶于水,不溶于醇类、乙醚等,加热至150℃左右开始分解放出氧气,与水缓慢反应生成H2O2.易于酸反应生成H2O2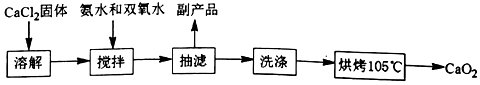
| 数据 时间 | 样品取用质量/(g) | 平均消耗体积(KMnO4)/mL |
| 放置前测定 | a | 25.00 |
| 放置一个月后测定 | a | 24.00 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | SO2,SiO2,P2O5 | B. | PCl3,CO2,H2SO4 | C. | SiC,H2O,NH3 | D. | HF,CO2,Si |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用高锰酸钾制取氧气 | |
| B. | 用氯酸钾和二氧化锰制取氧气 | |
| C. | 用锌和稀硫酸制取氢气 | |
| D. | 用石灰石和稀盐酸制取二氧化碳气体 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 两种溶液中的c(Na+)相等 | |
| B. | 分别加热到相同温度时,CH3COONa溶液的pH大 | |
| C. | 分别加水稀释到100 mL时,两种溶液的pH依然相等 | |
| D. | 两溶液中由水电离出的c(OH-)之比为$\frac{1{0}^{-5}}{1{0}^{-9}}$ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com