
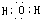
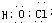 ,氢原子与活泼金属反应时,能够得1个电子形成负1价氢离子,形成离子化合物,NaH的电子式为:
,氢原子与活泼金属反应时,能够得1个电子形成负1价氢离子,形成离子化合物,NaH的电子式为: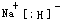 ,氢原子可得1个电子,生成稳定的负1价氢离子,类似于VIIA的元素,
,氢原子可得1个电子,生成稳定的负1价氢离子,类似于VIIA的元素,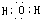
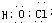 ;
;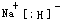 ;VIIA;
;VIIA;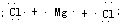 →
→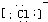
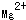
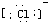 ,故答案为:
,故答案为: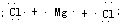 →
→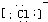
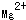
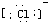 .
.


科目:高中化学 来源: 题型:
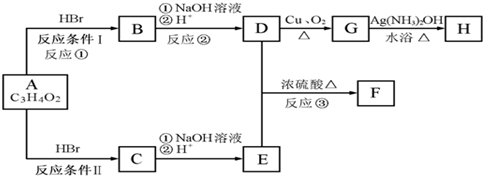
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、给试管内的液体加热,可使试管口对准自己,不能对准别人 |
| B、用规格为50 mL的量筒量取2.5 mL的液体 |
| C、称量NaOH固体的质量时,把NaOH固体直接放到天平左边的托盘上 |
| D、实验室制取氧气时,先检查装置的气密性,然后再加药品 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、Na2S、Na2SO3、AgNO3、NaCl、NaOH |
| B、HCHO、CuSO4、NaOH、FeCl2、FeSO4 |
| C、Br2、CH3CHO、CH3COOH、Ag(NH3)2Cl、NaHCO3 |
| D、KAl(SO4)2、NaHSO4、Al2(SO4)3、KCl、MgCl2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、③ | B、③④ | C、②③ | D、①⑤ |
查看答案和解析>>
科目:高中化学 来源: 题型:
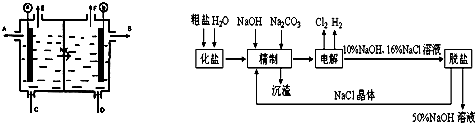
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
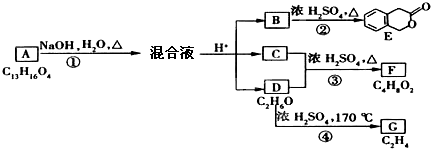
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、具有相似的化学性质 |
| B、具有相同的物理性质 |
| C、分子具有相同的空间结构 |
| D、分子式相同,碳原子的空间结构不同 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com