
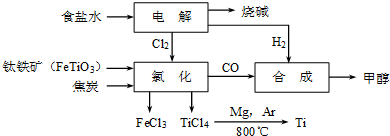
��12�֣���ұ�������ȼ���״������һ����ҵ������ͼ��ʾ��������������Դ�������ʣ����ٻ�����Ⱦ��

��ش��������⣺
��1��Ti��ԭ������Ϊ22��Tiλ��Ԫ�����ڱ��е�_______���ڣ���______�塣
��2��д���������ڸ������뽹̿���Ȼ��õ����Ȼ��ѵĻ�ѧ����ʽ ��
��3���Ʊ�TiO2�ķ���֮һ������TiCl4ˮ������TiO2��x H2O���پ������Ƶá�ˮ��ʱ����������ˮ�����ȣ����ϻ�ѧ����ʽ�ͱ�Ҫ������˵��ԭ��
��4����TiCl4��Ti ��Ҫ��Ar���н��е�������_________________________________����Ӧ��õ�Mg��MgCl2��Ti�Ļ����ɲ����������ķ�������õ�Ti�������±���Ϣ������ȵ��¶��Ը��� �漴�ɡ�
|
|
TiCl4 |
Mg |
MgCl2 |
Ti |
|
�۵�/�� |
��25.0 |
648.8 |
714 |
1667 |
|
�е�/�� |
136.4 |
1090 |
1412 |
3287 |
��5����������ԭ�ζ����ⶨTiO2������������һ�������£���TiO2�ܽⲢ��ԭΪTi3+������KSCN��Һ��ָʾ������NH4Fe(SO4)2����Һ�ζ�Ti3+��ȫ������Ti4+���ζ�����ʱ����ȡTiO2��Ħ������ΪM g/mol������w g������c mol/L NH4Fe(SO4)2����ҺV mL����TiO2��������Ϊ___________________�����ô���ʽ��ʾ��
��6����CO��H2�ϳɼ״��ķ���ʽ�ǣ�CO(g)��2H2(g) CH3OH(g)���������������� �������ʵ��κ���ʧ��������ҵ����ÿ�ϳ�6mol�״�����������ⲹ��H2 mol��
CH3OH(g)���������������� �������ʵ��κ���ʧ��������ҵ����ÿ�ϳ�6mol�״�����������ⲹ��H2 mol��
����12�֣�ÿС��2�֣�
��1����;��B����1�֣�
��2��2FeTiO3��6C��7Cl2���� 2FeCl3��2TiCl4��6CO
��3��TiCl4+(2+x) H2O TiO2��xH2O+4HCl���������ˮ�����ȣ��ٽ�ˮ��������ȫ�����ʹˮ���������
TiO2��xH2O+4HCl���������ˮ�����ȣ��ٽ�ˮ��������ȫ�����ʹˮ���������
��4����ֹ�ѡ�þ�����������ֹ��þ�������ˮ��Ӧ����1412
��5��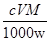 ����
����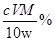 ��
��
��6��5
��������
�����������1��Ti��ԭ������Ϊ22����K��3����Kͬ��������K����3������2����ͼʾ��֪�Ȼ�ʱ�ķ�Ӧ�������ٸ��ݵ�ʧ���Ӻ�ԭ���غ㼴�ɵó��÷�Ӧ�ķ���ʽ����5�����ݵ�ʧ�����غ㣺1Ti3+��1Fe3+����n��Fe3+��=n��Ti3+��=n��TiO2��=cV��10-3mol������������Ϊ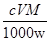 ����
����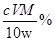 ����
����
���㣺���ʵ��ת�����Ʊ���ѧ������д��ѧ����ʽ
������������һ���йص��ԭ����Ӧ��֪ʶ��Ŀ��Ҫ��ѧ�����з����ͽ��������������ѶȽϴ����ָ�ڵ����У�ֱ����ͨ���缫�͵���ʣ������߽Ӵ��Ľ����Ϸ����绯ѧ��Ӧ�����Ʊ������Ʒ�Ĺ��̡�ѧϰ���ԭ��Ӧע�����¼���Ҫ�㡣һ��ע���������жϡ������ķ�Ӧ�����ӷ���ʽ����дȷ�����ص��������������ӵ�Դ������������,��缫������,���Դ���������ĵ缫Ϊ����,���Դ���������ĵ缫Ϊ����������������Ӧ:����:��������������,������ԭ��Ӧ;����:�������������ƶ�,����������������Ӧ,�缫����Ҳ���Է���������Ӧ;���ӷŵ�˳��:������:S2->I->Br->Cl->OH->�����������;������:Ag+>Cu2+>H+������


 ���Ͱ�ͨ��ĩ���ϵ�д�
���Ͱ�ͨ��ĩ���ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ��Ķ�����
 ��
��
| ||
| ||
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�


�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| TiCl4 | Mg | MgCl2 | Ti | |
| �۵�/�� | -25.0 | 648.8 | 714 | 1667 |
| �е�/�� | 136.4 | 1090 | 1412 | 3287 |
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com