
| A.0.5mol/(L?min) | B.2.5mol/(L?min) |
| C.2mol/(L?min) | D.5mol/(L?min) |
科目:高中化学 来源:不详 题型:问答题
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| 1 |
| 3 |
| 2 |
| 3 |
| 1 |
| 2 |
| 1 |
| 2 |
| A.196.46kJ | B.55.175kJ | C.141.285kJ | D.282.57kJ |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.υ(W)=υ(Z) | B.3υ(W)=2υ(X) | C.2υ(X)=υ(Y) | D.3υ(W)=4υ(Y) |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.等于10s | B.等于12s | C.大于12s | D.小于12s |
查看答案和解析>>
科目:高中化学 来源:不详 题型:多选题
| A.Z为0.3mol/L | B.Y2为0.35mol/L |
| C.X2为0.2mol/L | D.Z为0.4mol/L |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.v(A)=0.2mol/(L?min) | B.v(B)=0.6mol/(L?min) |
| C.v(C)=0.5mol/(L?min) | D.v(D)=0.01mol/(L?s) |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
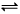 2C(g) ,下列关于该反应达到平衡状态的标志的说法中不正确的是
2C(g) ,下列关于该反应达到平衡状态的标志的说法中不正确的是 查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
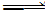 2SO3(g);ΔH=-197.74 kJ·mol-1。
2SO3(g);ΔH=-197.74 kJ·mol-1。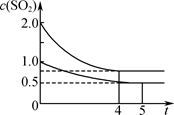
| A.热量:Q(甲)<2Q(乙) |
| B.压强:p(甲)<2p(乙) |
| C.乙中前5 min内的反应速率v(O2)=0.10 mol·L-1·min-1 |
| D.保持其他条件不变,若起始时向乙中充入0.4 mol SO2、0.2 mol O2、0.4 mol SO3,则此时v(正)<v(逆) |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com