
| ||
| n |
| V |
| ||
| 0.00075mol |
| 0.075L |
| 1×10 -14 |
| 0.01 |


 开心蛙口算题卡系列答案
开心蛙口算题卡系列答案科目:高中化学 来源: 题型:
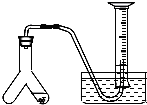 在室温和大气压强下,用图示的装置进行实验,测得a g含CaC2 90%的样品与水完全反应产生的气体体积为b L.现欲在相同条件下,测定某电石试样中CaC2的质量分数,请回答下列问题:
在室温和大气压强下,用图示的装置进行实验,测得a g含CaC2 90%的样品与水完全反应产生的气体体积为b L.现欲在相同条件下,测定某电石试样中CaC2的质量分数,请回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| 二甲苯一溴代物的熔点(℃) | 234 | 206 | 214 | 204 | 212 | 205 |
| 对应的二甲苯的熔点(℃) | 13 | -48 | -25 | -48 | -25 | -48 |
| A、熔点为234℃的是一溴代间二甲苯 |
| B、熔点为234℃的是一溴代邻二甲苯 |
| C、熔点为-48℃的是间二甲苯 |
| D、熔点为-25℃的是对二甲苯 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 水① |
| ② |
| ③ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、Al粉与NaOH溶液反应 Al+2OH-=AlO-2+H2↑ |
| B、表示稀盐酸和氢氧化钠稀溶液的热化学方程式 HCl+NaOH=NaCl+H2O;△H=-57.3 kJ/mol |
| C、明矾净水原理的离子方程式 Al3++3H2O=Al(OH)3+3H+ |
| D、硫酸铵浓溶液与氢氧化钠浓溶液混合的离子方程式NH4++OH-=NH3↑+H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、乙酸乙酯和水、酒精和水 |
| B、二溴乙烷和水、溴苯和水、 |
| C、甘油和水、乙酸和乙醇 |
| D、油酸和水、己烷和苯 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、2种 | B、3种 | C、4种 | D、5种 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、需要加热方能发生的反应一定是吸热反应 |
| B、放热的反应在常温下一定很易发生 |
| C、一个反应是放热反应还是吸热反应主要由反应物、生成物所具有的总能量的相对大小决定,而不是由反应是否需要加热而决定 |
| D、吸热反应发生过程中要不断从外界获得能量、放热反应发生过程中不再需要外界能量 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com