
在一个不导热的密闭反应器中,只发生两个反应:
a(g)+b(g) 2c(g);△H1<0
2c(g);△H1<0
x(g)+3y(g) 2z(g);△H2>0
2z(g);△H2>0
进行相关操作且达到平衡后(忽略体积改变所作的功),下列叙述错误的是
A.等压时,通入惰性气体,c的物质的量不变
B.等压时,通入z气体,反应器中温度升高
C.等容时,通入惰性气体,各反应速率不变
D.等容时,通入z气体,y的物质的量浓度增大
科目:高中化学 来源:2016-2017学年江苏省高一上期中化学卷(解析版) 题型:选择题
氧化还原反应与四种基本反应类型的关系如下图所示,则下列化学反应属于丙区域的是( )

A.Cl2+2KBr=Br2+2KCl
B.2NaHCO3 Na2CO3+H2O+CO2↑
Na2CO3+H2O+CO2↑
C.3Mg+N2 Mg3N2
Mg3N2
D.2Na2O2+2CO2=2Na2CO3+O2
查看答案和解析>>
科目:高中化学 来源:2016-2017学年黑龙江双鸭山一中高二上期中化学卷(解析版) 题型:选择题
对于反应:4CO(g)+2NO2(g)= 4CO2(g)+N2(g) △H=-1200 kJ· mol-1,温度不同 (T2>T1)其他条件相同时,下列图像正确的是
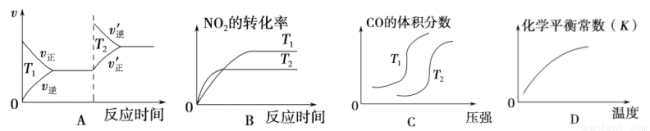
查看答案和解析>>
科目:高中化学 来源:2016-2017学年黑龙江大庆一中高二上11月月考化学卷(解析版) 题型:实验题
高铁酸盐在能源、环保等方面有着广泛的用途。湿法、干法制备高铁酸盐的原理如下表所示。
湿法 | 强碱性介质中,Fe(NO3)3与NaClO反应生成紫红色高铁酸盐溶液 |
干法 | Fe2O3、KNO3、KOH混合加热共熔生成紫红色高铁酸盐和KNO2等产物 |
(1)工业上用湿法制备高铁酸钾(K2FeO4)的流程如下图所示 :
:

①洗涤粗品时选用异丙醇而不用水的理由是: 。
②反应Ⅱ的离子方程式为 。
③高铁酸钾在水中技能消毒杀菌,又能净水,是一种理想的水处理剂,它能消毒杀菌是因为 ,它能净水的原因是因为 。
④已知25℃时Fe(OH)3的Ksp = 4.0×10-38,反应II后的溶液c(Fe3+)=4.0×10-5mol/L,则需要调整到 时,开始生成Fe(OH)3(不考虑溶液体积的变化)。
(2)由流程图可见,湿法制备高铁酸钾时,需先制得高铁酸钠,然后再向高铁酸钠中加入饱和KOH溶液,即可析出高铁酸钾。
①加入饱和KOH溶液的目的是 。
②由以上信息可知:高铁酸钾的溶解度比高铁酸钠 (填“大”或“小”)。
(3)干法制备K2FeO4的反应中氧化剂与还原剂的物质的量之比为 。
查看答案和解析>>
科目:高中化学 来源:2016-2017学年黑龙江大庆一中高二上11月月考化学卷(解析版) 题型:选择题
常温下,下列各组离子在指定溶液中一定能大量共存的是
A.0.1mol/L FeCl3溶液:K+、NH4+、SCN-、NO3-
B.0.1mol/LCu(NO3)2溶液:Na+、Mg2+、Cl-、SO42-
C.0.5mol/L AlCl3溶液:K+、Na+、S2-、SO42-
D.由水电离产生的c(H+)=10-13 mol·L-1的溶液:K +、Na+、HCO3-、Cl-
查看答案和解析>>
科目:高中化学 来源:2016-2017学年黑龙江大庆一中高二上11月月考化学卷(解析版) 题型:选择题
某温度下在密闭容器中发生如下反应:2M(g)+N(g)  2E(g)若开始时只充入2 mol E(g),达平衡时,混合气体的压强比起始时增大了20%。若开始时只充入2 mol M和1 mol N的混合气体,达平衡时M的转化率为
2E(g)若开始时只充入2 mol E(g),达平衡时,混合气体的压强比起始时增大了20%。若开始时只充入2 mol M和1 mol N的混合气体,达平衡时M的转化率为
A.20% B.40% C.60% D.80%
查看答案和解析>>
科目:高中化学 来源:2016-2017学年山西省高一上期中化学试卷(解析版) 题型:实验题
实验室配制480Ml0.1mol/LNa2CO3溶液,请回答下列问题:
(1)配制480Ml0.1mol/LNa2CO3溶液时,需要Na2CO3固体的质量为________g。
(2)配制过程中所需的仪器除药匙、天平、烧杯、量筒、玻璃棒、胶头滴管外,还需要________仪器。若在称量样品时,药品放在天平右盘上,砝码放在天平左盘上,1g以下用游码,天平平衡时,则实际称量的十水合碳酸钠质量________(填符号 A偏高 B偏低 C不变)
(3)配制时,其正确的操作顺序是_______(天字母);
A、用30mL蒸馏水洗涤烧杯和玻璃棒各2-3次,洗涤液均注入容量瓶中,震荡
B、用托盘天平准确称量所需的Na2CO3的质量,放入烧杯中,再加入少量蒸馏水(约30mL),用玻璃棒慢慢搅动,使其完全溶解
C、将已冷却至室温的Na2CO3溶液沿玻璃棒注入一定规格的容量瓶中
D、将容量瓶盖紧,震荡,摇匀
E、改用胶头滴管滴加蒸馏水,使溶液凹液面最低点恰好与刻度线相切
F、继续往容量瓶内加入蒸馏水,直到液面距刻度线1~2㎝处
(4)若出现以下情况,对所配溶液浓度将有何影响(填“偏高”、“偏低”或“无影响”)?
①没有进行A操作____________。
②家蒸馏水时不慎超过了刻度线____________。
③定容时俯视刻度线____________。
④溶液未恢复至室温就注入容量瓶____________。
查看答案和解析>>
科目:高中化学 来源:2016-2017学年山西省高一上期中化学试卷(解析版) 题型:选择题
下列配制的溶液浓度偏高的是
A.配制盐酸溶液,用量筒量取盐酸时俯视刻度线
B.配制盐酸溶液定容时,仰视容量瓶
C.称量40gNaOH配制0.20mol/LNaOH溶液500mL时,砝码错放左盘
D.配制NaOH溶液时,溶液未经冷却即注入容量瓶并定容至刻度线
查看答案和解析>>
科目:高中化学 来源:2016-2017学年山西省高二上11月月考化学卷(解析版) 题型:选择题
下列固体物质溶液水,再将其溶液加热,蒸发结晶、再灼烧,能得到化学组成与原固体物质相同的是①胆矾 ②氯化铝 ③硫酸铝 ④NaHCO3 ⑤氯化铜
A.③④ B.①③④ C.①②③④ D.全部
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com