
下列实验中,所采取的分离方法与对应原理都正确的是
选项 | 目的 | 分离方法 | 原理 |
A | 除去KNO3固体中混杂的NaCl | 重结晶 | NaCl在水中的溶解度很大 |
B | 氯气中混有氯化氢气体 | 洗气 | 氯气和氯化氢在饱和食盐水中溶解度不同 |
C | 除去苏打中少量小苏打 | 加热 | 二者的溶解度不同 |
D | 分离CCl4和碘的混合溶液 | 升华 | 乙醇与乙酸沸点相差较大 |
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源:2015-2016学年广东省高一上学期10月月考化学试卷(解析版) 题型:选择题
下列说法不正确的是
A.检验Cl-离子的试剂是硝酸银和硝酸
B.配制一定物质的量浓度溶液时,未洗涤烧杯和玻璃棒,结果会偏低
C.配制一定物质的量浓度溶液时,容量瓶中有少量蒸馏水,对浓度无影响
D.向溶液中加入BaCl2溶液后生成白色沉淀,即可证明有SO42-
查看答案和解析>>
科目:高中化学 来源:2015-2016学年河南省高二上学期第二次月考化学试卷(解析版) 题型:选择题
pH=2的两种一元酸x和y,体积均为100 mL,稀释过程中pH与溶液体积的关系如图所示。分别滴加NaOH溶液(c=0.1 mol/L)至pH=7,消耗NaOH溶液的体积为Vx、Vy,则
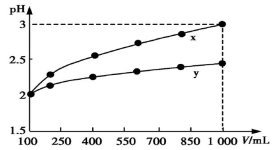
A.x为弱酸,Vx<Vy B.x为强酸,Vx>Vy
C.y为弱酸,Vx<Vy D.y为强酸,Vx>Vy
查看答案和解析>>
科目:高中化学 来源:2016届宁夏长庆高级中学高三上学期第三次月考理综化学试卷(解析版) 题型:填空题
化学实验的微型化可有效地减少污染,实现化学实验绿色化的要求。某学生按下列操作做一个实验:在一块下衬白纸的玻璃片的不同位置分别滴加浓度为0.1 mol/L的KBr、KI(含淀粉溶液)、NaOH(含酚酞)、FeCl2(含KSCN)溶液各1滴,每种液滴彼此分开,围成半径小于表面皿的圆形(如图所示),在圆心处放置2粒芝麻粒大小的KMnO4晶体,向KMnO4晶体滴加一滴浓盐酸,再立即将表面皿盖好。
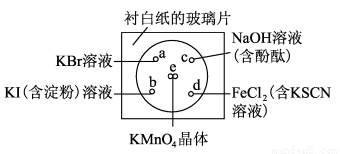
(1)请配平e处的化学反应方程式
 KMnO4+
KMnO4+ HCl(浓)===
HCl(浓)=== KCl+
KCl+ MnCl2+
MnCl2+ Cl2↑+
Cl2↑+ H2O
H2O
(2)e处反应中发生氧化还原反应的氧化剂和还原剂的物质的量之比为 。
(3)b处的实验现象为 ,d处的离子方程式为 。
(4)c处反应的离子方程式为 ,标准状况下,当有0.224 L Cl2被NaOH溶液吸收后,转移电子的物质的量为________mol。
(5)通过该实验能否比较Cl2、FeCl3、KMnO4三种物质氧化性的强弱?________(填“能”或“不能”),若能,其氧化性由强到弱的顺序是______________________。
查看答案和解析>>
科目:高中化学 来源:2016届四川省绵阳市高三上学期第一次诊断性测试理综化学试卷(解析版) 题型:实验题
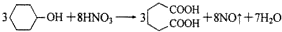
己二酸是合成尼龙-66的主要原料之一。实验室合成己二酸的原理、有关数据及装置示意图如下:
物质 | 密度(g/cm3) | 熔点 | 沸点 | 溶解性 |
环己醇 | 0.962g/cm3 | 25.9℃ | 160.8℃ | 20℃时水中溶解度为3.6g,可混溶于乙醇、苯 |
己二酸 | 1.360g/cm3 | 152℃ | 337.5℃ | 在水中的溶解度:15℃时1.44g,25℃时2.3g,易溶于乙醇、不溶于苯 |
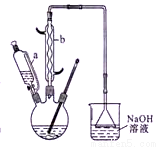
实验步骤如下:
I.在三口烧瓶中加入16 mL 50%的硝酸(密度为l.3lg/cm3),再加入1~2粒沸石,滴液漏斗中盛放有5.4 mL环己醇。
II.水浴加热三口烧瓶至50℃左右,移去水浴,缓慢滴加5~6滴环己醇,摇动三口烧瓶,观察到有红棕色气体放出时再慢慢滴加剩下的环己醇,维持反应温度在60℃~65℃之间。
Ⅲ.当环己醇全部加入后,将混合物用80℃一90℃水浴加热约10min(注意控制温度),直至无红棕色气体生成为止。
Ⅳ,趁热将反应液倒入烧杯中,放入冰水浴中冷却,析出晶体后过滤、洗涤、干燥、称重。
请回答下列问题:
(1)本实验所用50%的硝酸物质的量浓度为__________。滴液漏斗的细支管a的作用是 。
(2)仪器b的名称为____ 使用时要从________(填“上口”或“下口”)通入冷水。
(3)NaOH溶液的作用是__________,溶液上方倒扣的漏斗作用是 。
(4)向三口烧瓶中滴加环己醇时,反应温度迅速上升,为使反应温度不致过高,必要时可采取的措施是 。
(5)进行该实验时要控制好环己醇的滴入速率,防止反应过于剧烈,否则可能造成较严重的后果,试列举两条可能的后果: 。
(6)为了除去可能的杂质和减少产品损失,可分别用__________和____________洗涤晶体。
查看答案和解析>>
科目:高中化学 来源:2015-2016学年福建省龙海市高二上学期期中测试化学试卷(解析版) 题型:选择题
在2A+B  3C+4D反应中,表示该反应速率最快的是
3C+4D反应中,表示该反应速率最快的是
A.v(A)=0.5 mol·L-1·s-1
B.v(B)=0.3 mol·L-1·s-1
C.v(C)=0.8 mol·L-1·s-1
D.v(D)=1 mol·L-1·s-1
查看答案和解析>>
科目:高中化学 来源:2015-2016学年湖北省黄石市高一上11月期中月考化学试卷(解析版) 题型:填空题
图1是某学校实验室从化学试剂商店买回的浓硫酸试剂标签上的部分内容。
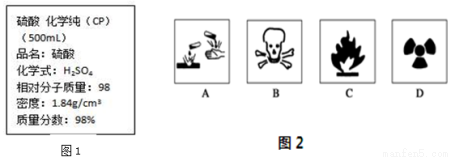
Ⅰ.(1)在盛放浓硫酸的试剂瓶的标签上应印有图2警示标志中的____________。
(2)若将该浓硫酸与等质量的水混合,则所得溶液中溶质物质的量浓度_________9.2mol/L(填>、<、=)。
Ⅱ.现欲用该浓硫酸配制成1mol/L的稀硫酸,现实验室仅需要这种稀硫酸220mL。试回答下列问题:
(3)用量筒量取该浓硫酸______________ mL。
(4)配制时,必须使用的仪器除量筒、烧杯外,还缺少的仪器是_________________。
(5)若在稀释过程中,浓硫酸不慎沾在手上,处理方法为 。
(6)配制溶液的过程中,其他操作都正确,下列操作会使所配溶液浓度偏高的是____________。
A.用量筒量取浓硫酸时俯视
B.稀释浓硫酸时,未冷却到室温即转移到容量瓶中
C.量取浓H2SO4后的量筒进行洗涤,并将洗涤液转移到容量瓶中
D.定容摇匀后,发现液面低于刻度线,又用胶头滴管加蒸馏水至凹液面最低处与刻度线相切
E.容量瓶不干燥
F.定容时,俯视容量瓶刻度线
查看答案和解析>>
科目:高中化学 来源:2015-2016学年上海市高二上学期期中测试化学试卷(解析版) 题型:选择题
Fe3O4与HNO3反应生成Fe(NO3)3、NO、H2O若溶解1mol Fe3O4,则被还原的硝酸是
A、3 mol B、1/2 mol C、1/3 mol D、9 mol
查看答案和解析>>
科目:高中化学 来源:2015-2016学年浙江余姚中学高一上学期期中考试化学试卷(解析版) 题型:选择题
下列叙述中,正确的是
A.次氯酸能杀死病菌,所以氯气可用于自来水的消毒
B.实验室制取氯气时,常用水来吸收多余的氯气
C.漂白粉中含有次氯酸,所以漂白粉能使染料等有机色素褪色
D.氯气不能使干燥的有色布条褪色,液氯能使干燥的有色布条褪色
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com