
 CH3COOH+OH-, H2O
CH3COOH+OH-, H2O H++OH-
H++OH-

 海淀黄冈名师导航系列答案
海淀黄冈名师导航系列答案 普通高中同步练习册系列答案
普通高中同步练习册系列答案科目:高中化学 来源:不详 题型:单选题
| A.氯化镁水解是熵增反应 | B.硫酸镁晶体分解反应是放热反应 |
| C.硫酸镁晶体分解反应是熵减反应 | D.氯化镁分解放热比硫酸镁少 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
A.CH3COO— + H2O CH3COOH + OH— CH3COOH + OH— | B.NH4+ + H2O NH4OH + H+ NH4OH + H+ |
C.S2—+ 2H2O H2S + 2 OH— H2S + 2 OH— | D.Cu2+ + 2H2O=Cu(OH)2↓+ 2H+ |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题


A.Va=Vb时:c (CH3COO-)="c" (K+) | B.Va=Vb时:c (CH3COOH) +c (H+)="c" (OH-) | C.Va>Vb时:c (CH3COO-)>c (K+)> c (OH-)> c (H+) | D.Va与Vb任意比时:c (K+)+ c (H+) =c (OH-)+ c (CH3COO-) |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
 NH4++OH- ②HCO3- + H2O
NH4++OH- ②HCO3- + H2O H2CO3+OH-
H2CO3+OH- H3O++CO32- ④A13+ +3HCO3-=Al(OH)3↓+3CO2↑
H3O++CO32- ④A13+ +3HCO3-=Al(OH)3↓+3CO2↑ NH3·H2O+H3O+
NH3·H2O+H3O+| A.①③⑤ | B.②③⑤ | C.①④⑤ | D.①③ |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题

| A.a点表示的溶液中由水电离出的H+浓度为1.0×10-11 mol·L-1 |
| B.b点表示的溶液c(CH3COO-) > c(Na+) |
| C.c点表示CH3COOH和NaOH恰好反应完全 |
D.b、d点表示的溶液中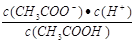 相等 相等 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com