
| A. | HCl | B. | 冰醋酸 | C. | Na2SO4 | D. | KOH |
分析 一般来说,活泼金属和活泼非金属元素之间存在离子键、非金属元素之间存在共价键,分子晶体和原子晶体中存在共价键、离子晶体中存在离子键,分子晶体熔化时破坏分子间作用力、原子晶体熔化时破坏共价键、离子晶体熔化时破坏离子键.
解答 解:A.HCl属于分子晶体,熔化时破坏分子间作用力,溶于水发生电离破坏共价键,所以破坏的作用力不同,故A错误;
B.冰醋酸分子晶体,熔化时破坏分子间作用力,溶于水发生电离破坏共价键,所以破坏的作用力不同,故B错误;
C.Na2SO4属于离子晶体,熔化时破坏离子键,溶于水发生电离破坏离子键,所以破坏的作用力相同,故C正确;
D.KOH属于离子晶体,熔化时破坏离子键,溶于水发生电离破坏离子键,所以破坏的作用力相同,故D正确.
故选CD.
点评 本题考查了化学键和分子间作用力,题目难度不大,注意分子晶体熔化时破坏分子间作用力,化学键不变.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:选择题
| A. | ①②③④ | B. | ④⑥⑧ | C. | ⑦⑧⑨ | D. | ⑤⑥⑦⑧ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 锌锰干电池工作一段时间后碳棒变细 | |
| B. | 铅蓄电池工作一段时间后酸性会增强 | |
| C. | 水和水煤气都是一级能源 | |
| D. | 铁与H2SO4反应时,加入少量CuSO4溶液时,可使反应加速 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
| 实 验 现 象 | 可 以 肯 定 的 结 论 |
| A、观察混合气体无色 | 无Cl2、 |
| B、将混合气体通过浓H2SO4,体积减小 | 有NH3、无HCl |
| C、剩余气体跟空气接触后变为红棕色 | 有NO、无O2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 原子半径:Na<Mg<Al | B. | 热稳定性:HCl>H2S>PH3 | ||
| C. | 酸性强弱:H2SiO3<H2CO3<HNO3 | D. | 碱性强弱:KOH>NaOH>LiOH |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 若某温度下,反应后$\frac{c(C{l}^{-})}{c(Cl{O}^{-})}$=11,则溶液中$\frac{c(Cl{O}^{-})}{c(Cl{{O}_{3}}^{-})}$=$\frac{1}{2}$ | |
| B. | 参加反应的氯气的物质的量小于$\frac{1}{2}$a mol | |
| C. | 改变温度,反应中转移电子的物质的量ne的范围:$\frac{1}{2}$a mol≤ne≤$\frac{5}{6}$a mol | |
| D. | 改变温度,产物中KC1O3的最大理论产量为$\frac{1}{7}$a mol |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 56g N2与12g H2在密闭容器中反应,转移电子的数目为12.0×6.02×1023. | |
| B. | 标准状况下,22.4L NO和11.2L O2混合后气体的分子总数为6.02×1023 | |
| C. | 工业上用电解法进行粗铜精炼时,每转移1mol电子,阳极上溶解的铜原子必为0.5×6.02×1023 | |
| D. | V L a mol•L-1 氯化铁溶液中,若Fe3+的数目为6.02×1023,则Cl-的数目大于3×6.02×1023 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | 有机物X的含氧官能团有3种 | |
| B. | X分子中苯环上的一氯取代物有3种 | |
| C. | 在Ni作催化剂的条件下,1mol X 最多能与5 mol H2加成 | |
| D. | X在一定条件下能发生加成、取代、消去等反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
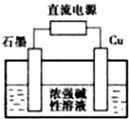 金属单质及其化合物在工农业生产中应用广泛.
金属单质及其化合物在工农业生产中应用广泛.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com