
��15�֣� ����ѧһѡ�� 5 ���л���ѧ������
�л������� A �����ϣ��������к�CΪ72��0 ����H Ϊ6��67 % ������Ϊ����������������֪ A ����Է�������Ϊ150�� A��һ��ͬ���칹��E����������������������㾫�ĵ������ϡ��������üױ����Ҵ�Ϊԭ�Ͻ����˹��ϳɡ��ϳ�·�����£�
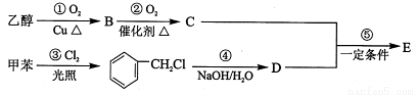
����գ�
��1��A�ķ���ʽΪ ��
��2��E�Ľṹ��ʽΪ ��
��3����Ӧ�ڢ۵ķ�Ӧ����Ϊ �� ��
��4��д����Ӧ�ٵĻ�ѧ����ʽ ��
��5��д����Ӧ�ܵĻ�ѧ����ʽ ��
��6��D�ķ�����ͬ���칹���� �֣����к˴Ź������ķ����֮��Ϊ1: 2 : 2 : 3������ͬ���칹��ṹ��ʽΪ ��
��1��C9H10O2����2��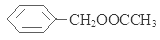 ����3��������Ӧ��ȡ����Ӧ��
����3��������Ӧ��ȡ����Ӧ��
��4��2CH3CH2OH+O2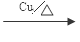 2CH3CHO+2H2O��
2CH3CHO+2H2O��
��5��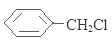 +NaOH
+NaOH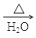
 +NaCl��
+NaCl��
��6��4 ��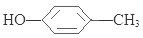 ��
�� ��
��
��������
�����������1����A�����к��и���Ԫ�ص�ԭ�Ӹ����ֱ��ǣ�C����150��72��0 ������12=9��H����150��6��67 %����1=10��O����150-12��9��1��10����16=2������A�ķ���ʽ�ǣ�C9H10O2����2���Ҵ��������õ�B��ȩCH3CHO��B�������õ�C����CH3COOH���ױ��������ڹ���ˮ����ȡ����Ӧ����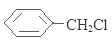 ��
��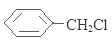 ��NaOH��ˮ��Һ����ȡ����Ӧ����D�����״�
��NaOH��ˮ��Һ����ȡ����Ӧ����D�����״� �����״���������Ũ���������·���������Ӧ����E�����ᱽ����
�����״���������Ũ���������·���������Ӧ����E�����ᱽ����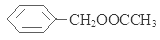 ��ˮ������E�Ľṹ��ʽΪ
��ˮ������E�Ľṹ��ʽΪ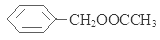 ;��3����Ӧ�ڵķ�Ӧ������������Ӧ����Ӧ�۵ķ�Ӧ����Ϊȡ����Ӧ����4����Ӧ�ٵĻ�ѧ����ʽ��2CH3CH2OH+O2
;��3����Ӧ�ڵķ�Ӧ������������Ӧ����Ӧ�۵ķ�Ӧ����Ϊȡ����Ӧ����4����Ӧ�ٵĻ�ѧ����ʽ��2CH3CH2OH+O2 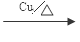 2CH3CHO+2H2O����5����Ӧ�ܵĻ�ѧ����ʽ��
2CH3CHO+2H2O����5����Ӧ�ܵĻ�ѧ����ʽ��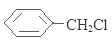 +NaOH
+NaOH 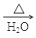
 +NaCl����6��D���״��ķ�����ͬ���칹�������֣��������ڼ����ӡ�������ӡ��Լ����Ӻͱ����ѣ����к˴Ź������ķ����֮��Ϊ1: 2 : 2 : 3��ͬ���칹���ǶԼ����Ӻͱ����ѣ����ǵĽṹ��ʽΪ
+NaCl����6��D���״��ķ�����ͬ���칹�������֣��������ڼ����ӡ�������ӡ��Լ����Ӻͱ����ѣ����к˴Ź������ķ����֮��Ϊ1: 2 : 2 : 3��ͬ���칹���ǶԼ����Ӻͱ����ѣ����ǵĽṹ��ʽΪ ��
�� ��
��
���㣺�����л���ķ���ʽ�ƶϡ����ʵĽṹ�����ʡ�ת������Ӧ���͡�����ʽ����д��ͬ���칹������༰�ṹ��ʽ����д��֪ʶ��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ��2015�����ʡ������һ���¿���ѧ�Ծ��������棩 ���ͣ�ѡ����
��NA��ʾ�����ӵ�����������������ȷ����( )
A����״̬�£�22.4 L C4H6�к���̼̼������һ��ΪNA
B����1molFeCl3�ı�����Һ�����ˮ�еõ�������������������ĿΪNA
C���ڱ�״���£�22.4 L����������������ΪNA
D��106 g Na2CO3�����е���������ΪNA
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015�����ʡ������ѧ����㿼�Ի�ѧ�Ծ��������棩 ���ͣ�ѡ����
������Ԫ��X��Y��Z��ԭ���������ε�������ԭ�ӵ�����������֮��Ϊ13��X��Y��Zλ���������ڣ�Zԭ��������������Xԭ���ڲ��������3��������Yԭ��������������3��������˵����ȷ����
A��X���⻯������ˮ�������� B��Z���⻯���ˮ��Һ�ڿ����д�Ų��ױ���
C��Y��X������Y3X2�ͻ����� D��Z�ĵ�����������ȼ�տ���������������������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015�����ʡ��������У�߶���ѧ������������ѧ�Ծ��������棩 ���ͣ�ѡ����
ij��������������Ӧ��������(CH3)2CHCH2CH3��������������� �� ��
A��2������2����ϩ B��3������1����ϩ
C��2��3��������1����ϩ D��3������1����Ȳ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015�����ʡ��������У�߶���ѧ������������ѧ�Ծ��������棩 ���ͣ�ѡ����
����Ԫ�����ʵĵݱ������ȷ����( )
A��ԭ�Ӱ뾶��Be<B<C<N
B����һ�����ܣ�B<Be<Mg<Na
C��Ԫ�صĵ縺�ԣ�O>N>P>Si
D����̬�⻯����ȶ��ԣ�NH3<CH4<PH3<SiH4
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015�����ʡ�¸��������в��Ի�ѧ�Ծ��������棩 ���ͣ������
( 9�֣��Թ�ҵ��ˮ��������ˮ���д����Ƿ�ֹˮ����Ⱦ������ˮ�ʵ���Ҫ��ʩ��
��1���������ƺͶ��ȷ�( )�ķ�ˮ����ͨ�����������س�ȥ����ԭ������ͼ��ʾ��
)�ķ�ˮ����ͨ�����������س�ȥ����ԭ������ͼ��ʾ��

��B�ǵ�ص� ��(���������)����A���ĵ缫��ӦʽΪ ��
��2��������������������������Һ��ͬʱ�õ������ԭ������ͼ��ʾ��ͼ�С�HA ����ʾ������ӣ�A����ʾ��������ӣ���
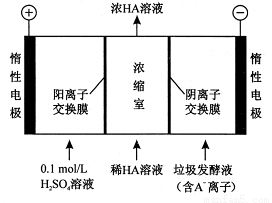
�������ĵ缫��ӦʽΪ ��
�ڼ���Ũ�����еõ�Ũ�����ԭ�� ��
�۵������У���ȡһ���Ĵ�ʩ�ɿ��������ҵ�pHԼΪ6~8 ����ʱ����Ũ���ҵ�OH���ɺ��Բ��ơ�400 mL10g/L ������Һͨ��һ��ʱ���Ũ������Ϊ 145g/L(��Һ����仯���Բ���)���������ϲ�����H2�ڱ�״���µ����ԼΪ L(�����Ħ������Ϊ90g/ mol ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015�����ʡ�¸��������в��Ի�ѧ�Ծ��������棩 ���ͣ�ѡ����
����˵����ȷ����
A��c( H+)��c(OH��)����Һһ�������� B�������£� pH = 6 ����Һһ��������Һ
C�����ϡ���������������Һ�IJ��ﲻͬ D������ˮ���ȣ���KW�����pH����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015�����ʡ������ѧ����㿼�Ի�ѧ�Ծ��������棩 ���ͣ�ѡ����
��֪NO2��N2O4�ת����2NO2��g�� N2O4��g������H=-24.4kJ/mol�ں����£���һ����NO2��N2O4��g���Ļ������������Ϊ2L���ܱ������У��������ʵ���Ũ����ʱ��仯�Ĺ�ϵ����ͼ���������������������ǣ� ��
N2O4��g������H=-24.4kJ/mol�ں����£���һ����NO2��N2O4��g���Ļ������������Ϊ2L���ܱ������У��������ʵ���Ũ����ʱ��仯�Ĺ�ϵ����ͼ���������������������ǣ� ��
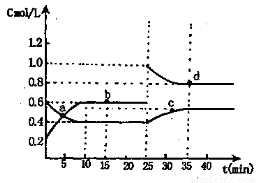
A��ǰ10min�ڣ���v��NO2����ʾ�ĸ÷�Ӧ����Ϊ0.02mol/��L��min��
B����Ӧ���е�10minʱ����ϵ���յ�����Ϊ9.76kJ
C��a��b��c��d�ĵ���v����v������
D��25minʱ������ƽ���ƶ���ԭ��������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015���㽭ʡЭ����߿����ײ��������ۺϻ�ѧ�Ծ��������棩 ���ͣ�ѡ����
��1����֪t ��ʱAgCl��Ksp��2��10��10 ����2����t ��ʱ��Ag2CrO4��ˮ�еij����ܽ�ƽ��������ͼ��ʾ������˵����ȷ���ǣ� ����

A����t ��ʱ��Ag2CrO4��KspΪ1��10��9
B���ڱ���Ag2CrO4��Һ�м���K2CrO4��ʹ��Һ��Y�㵽X��
C����t��ʱ����0.01 mol/L AgNO3��Һ�ζ�20 mL0.01 mol/LKCl��0.01 mol/L��K2CrO4�Ļ����Һ��Cl���ȳ���
D����t ��ʱ��AgCl���ܽ�ȴ���Ag2CrO4
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com