
| A.将乙醛加入含有新制银氨溶液的试管中,于沸水浴中加热来值得银镜 |
| B.称量12.5gCuSO4·5H2O,配成100mL溶液,得到0.5mol/L的CuSO4溶液 |
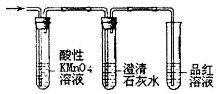
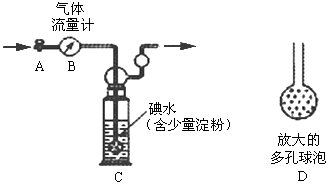
| C.用图1装置检验实验室制得的乙烯中混有SO2和CO2 |
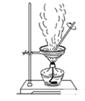
| D.利用图2装置从氯化铁溶液中直接蒸发结晶获得氯化铁晶体 |
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源:不详 题型:实验题
| A.用洁净的试管; |
| B.在浓度为2%的NH3·H2O中滴入稍过量的浓度为2%的硝酸银; |
| C.用前几天配制好的银氨溶液; |
| D.在银氨溶液里加入稍过量的甲酸; |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.酸性高锰酸钾溶液中通入SO2气体后,紫色消失 |
| B.滴有酚酞的氢氧化钠溶液中通入SO2后,红色消失 |
| C.品红溶液通入SO2后,红色消失 |
| D.溴水中通入SO2后,橙色消失 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
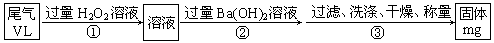
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
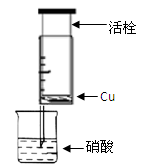
| 组 | m(Cu)/g | 硝酸(过量) | 溶液颜色 |
| A | 1 | 浓HNO3(4mL) | 溶液为绿色 |
| 1 | 稀HNO3(4mL) | 溶液为蓝色 | |
| B | 0.5 | 浓HNO3(4mL) | 溶液为绿色 |
| 1 | 稀HNO3(4mL) | 溶液为蓝色 | |
| C | 2 | 浓HNO3(4mL) | 溶液为绿色 |
| 1 | 稀HNO3(4mL) | 溶液为蓝色 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
| A.溶液中水电离出的OH-个数:②>① | B.溶液中阴离子的物质的量浓度之和:②>① |
| C.①溶液中:c(CO32-)>c(H2CO3) | D.②溶液中:c(HCO3-)>c(H2CO3) |
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
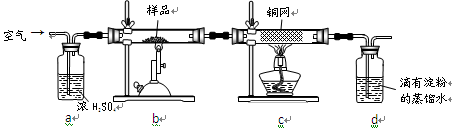
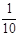 置于锥形瓶中,用0.05mol/L标准碘溶液进行滴定,初读数为0.10mL,末读数如右图所示。
置于锥形瓶中,用0.05mol/L标准碘溶液进行滴定,初读数为0.10mL,末读数如右图所示。

查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
 5NaC1+NaC1O3+3H2O,今在—5℃的NaOH溶液中通入适量C12(平衡常数K=1.09×1012),此时C12的氧化产物主要是 ;将溶液加热,溶液中主要离子浓度随温度的变化如右图所示,图中A、B、C依次表示的离子是 。
5NaC1+NaC1O3+3H2O,今在—5℃的NaOH溶液中通入适量C12(平衡常数K=1.09×1012),此时C12的氧化产物主要是 ;将溶液加热,溶液中主要离子浓度随温度的变化如右图所示,图中A、B、C依次表示的离子是 。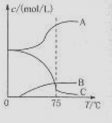
 NaC1O3+3H2↑
NaC1O3+3H2↑ HC1O+H++C1— HC1O
HC1O+H++C1— HC1O H++C1O—
H++C1O—
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com