
分析 (1)MnO2+4HCl(浓)$\frac{\underline{\;\;△\;\;}}{\;}$MnCl2+Cl2↑+2H2O中,Mn元素的化合价降低,Cl元素的化合价升高,4molHCl反应其中只有2molHCl被氧化生成1molCl2,以此来解答;
(2)反应3Cl2+6NaOH=5NaCl+NaClO3+3H2O中,Cl元素的化合价由0降低为-1价,由0升高为+5价,以此来解答.
解答 解:(1)MnO2+4HCl(浓)$\frac{\underline{\;\;△\;\;}}{\;}$MnCl2+Cl2↑+2H2O中,Mn元素的化合价降低,Cl元素的化合价升高,4molHCl反应其中只有2molHCl被氧化生成1molCl2,氧化剂是二氧化锰,HCl发生氧化反应;生成1mol Cl2时转移电子数目为2mol,被氧化的HCl的物质的量是2mol,盐酸显示的性质是还原性和酸性,故答案为:MnO2;HCl;2mol;2mol;还原性和酸性;
(2)反应3Cl2+6NaOH=5NaCl+NaClO3+3H2O中,因氯气中Cl元素的化合价既升高又降低,则Cl2既是氧化剂也是还原剂,氢氧化钠中各元素的化合价都不变,所以氢氧化钠既不是氧化剂又不是还原剂,3molCl2完全反应电子转移3mol×2×$\frac{5}{6}$(1-0)=5mol,氧化剂和还原剂的物质的量之比是5:1,故答案为:氧化剂、还原剂;5mol;5:1.
点评 本题考查氧化还原反应,把握反应中元素的化合价变化是解答本题的关键,侧重氧化还原反应中基本概念和电子转移的考查,题目难度不大.


科目:高中化学 来源: 题型:解答题
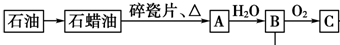
 ,它的一氯取代产物有2种.
,它的一氯取代产物有2种.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | SiO2和SO2 | B. | NaCl和HCl | C. | CO2和H2O | D. | CH4和KCl |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ②④ | B. | ②③ | C. | ①③ | D. | ①④ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| I1/KJ•mol-1 | I2/KJ•mol-1 | I3/KJ•mol-1 | I4/KJ•mol-1 | I5/KJ•mol-1 |
| 738 | 1451 | 7733 | 10540 | 13630 |
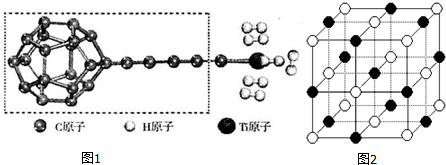
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
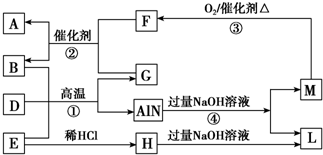
 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 原子半径:A<C<B | |
| B. | 2.32g四氧化三铁与足量的B完全反应转移0.09mol电子 | |
| C. | C的气态氢化物无毒 | |
| D. | A元素在周期表中位于第二周期第VIA族 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 乙烯使溴的四氯化碳溶液褪色 | |
| B. | 苯与浓硝酸、浓硫酸混合共热制取硝基苯 | |
| C. | 将苯滴入溴水中,振荡后水层接近无色 | |
| D. | 乙烯使KMnO4溶液褪色 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com