
【题目】如图所示,装置(Ⅰ)是一种可充电电池的示意图,装置(Ⅱ)为电解池的示意图;装置(Ⅰ)的离子交换膜只允许![]() 通过。电池放电的化学方程式为
通过。电池放电的化学方程式为![]() 。当闭合K时,X极附近溶液先变红色。下列说法正确的是( )
。当闭合K时,X极附近溶液先变红色。下列说法正确的是( )
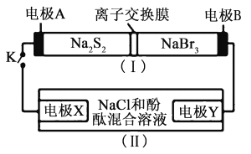
A.装置(Ⅰ)中A为正极
B.电极X的电极溶液变红的原因![]()
C.放电时,电极B的电极反应式为![]()
D.给原电池充电时![]() 从右向左通过离子交换膜
从右向左通过离子交换膜
 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
【题目】NaCl和NaClO在酸性条件下可发生反应:ClO-+Cl-+2H+=Cl2↑+H2O,某学习小组拟研究消毒液(主要成分为NaCl和NaClO)的变质情况。
(1)此消毒液中NaClO可吸收空气中的CO2生成NaHCO3和HClO。写出化学反应方程式___。
(2)取适量消毒液放在试管中,加入足量一定浓度的硫酸,有气体放出。通过以下装置检验气体的成分可以判断消毒液是否变质。
限选试剂:98%浓硫酸、1%品红溶液、1.0mol·L-1KI淀粉溶液、1.0mol·L-1NaOH溶液、澄清石灰水、饱和NaCl溶液。
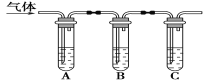
请完成下列实验方案。
所加试剂 | 预期现象和结论 |
试管A中加足量①___; 试管B中加1%品红溶液; 试管C中加②___。 | 若A中溶液变蓝色,B中溶液不褪色,C中溶液变浑浊,则消毒液部分变质;③___,则消毒液未变质;④___,则消毒液完全变质。 |
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铜板上铁铆钉长期暴露在潮湿的空气中,形成一层酸性水膜后铁铆钉会被腐蚀,示意图如下。下列说法不正确的是
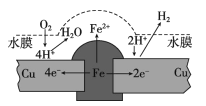
A. 腐蚀过程中铜极上始终只发生: 2H++2e-= H2↑
B. 若水膜中溶有食盐将加快铁铆钉的腐蚀
C. 若在金属表面涂一层油脂能防止铁铆钉被腐蚀
D. 若将该铜板与直流负极相连,则铁铜均难被腐蚀
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】电浮选凝聚法是工业上采用的一种污水处理方法:保持污水的pH在5.0~6.0,通过电解生成Fe(OH)3沉淀。Fe(OH)3有吸附性,可吸附污物而沉积下来,具有净化水的作用。阴极产生的气泡把污水中悬浮物带到水面形成浮渣层,弃去浮渣层,即起到了浮选净化的作用。某科研小组用电浮选凝聚法处理污水,设计的装置示意图如图1所示。
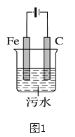
回答下列问题:
(1)电解过程中,电解池阴极的电极反应式为______;控制电流,可使电解池阳极同时发生两个电极反应:其中一个为2H2O -4e- === O2↑+ 4H+,另一个电极反应式为______。
(2)电解池溶液中得到Fe(OH)3沉淀的离子方程式为______。
(3)某熔融盐燃料电池以熔融的多种碱金属碳酸盐混合物为电解质,CH4为燃料,空气为氧化剂,稀土金属材料为电极,如图2。若该熔融盐燃料电池为电浮选凝聚法的电解电源,则:
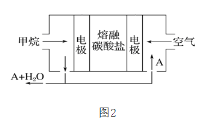
①正极的电极反应式为______;
②为了使该燃料电池长时间稳定运行,电池的电解质组成应保持稳定。为此电池工作时必须有部分A物质参加循环。则A物质的化学式是______。
③实验过程中,若在阴极产生了44.8L(标准状况)气体,则熔融盐燃料电池理论上消耗CH4______L(标准状况)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】CO与N2O是汽车尾气中污染大气的成分,研究表明CO与N2O在Fe+作用下生成无害气体,发生反应的能量变化及反应历程如图所示,两步反应分別为:① N2O+Fe+=N2+FeO+(慢);② FeO++CO=CO2+Fe+(快)。下列说法不正确的是( )
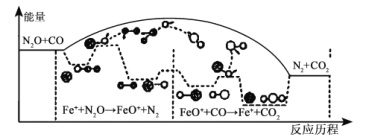
A.①是氧化还原反应,②不是氧化还原反应
B.两步反应均为放热反应,总反应的化学反应速率由反应①决定
C.Fe+使反应的活化能减小,增大反应速率
D.FeO+在该反应过程中作催化剂
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某工业废水中存在大量的Na+、Cl-、Cu2+、SO42-,欲除去其中的Cu2+、SO42-,设计工艺流程如图所示:

下列说法不正确的是
A.NaOH的作用是除去Cu2+B.试剂a 为Na2CO3,试剂b为BaCl2
C.流程图中,操作x为过滤D.试剂c为盐酸
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某小组同学通过实验研究FeCl3溶液与Cu粉发生的氧化还原反应。实验记录如下:
序号 | I | II | III |
实验步骤 |
充分振荡,加2mL蒸馏水 |
充分振荡,加入2mL蒸馏水 |
充分振荡,加入2mL蒸馏水 |
实验现象 | 铜粉消失,溶液黄色变浅,加入蒸馏水后无明显现象 | 铜粉有剩余,溶液黄色褪去,加入蒸馏水后生成白色沉淀 | 铜粉有剩余,溶液黄色褪去, 变成蓝色,加入蒸馏水后无白色沉淀 |
下列说法不正确的是( )
A.实验I、II、III中均发生了反应2Fe3++Cu=2Fe2++Cu2+
B.对比实验I、II、III说明白色沉淀的产生可能与铜粉的量及溶液的阴离子种类有关
C.实验I、III中加入蒸馏水后c(Cu2+)相同
D.向实验III反应后的溶液中加入饱和NaCl溶液可能出现白色沉淀
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以饱和食盐水、NH3和CO2为原料,可以制取纯碱。下列说法正确的是( )
A.由反应N2(g)+3H2(g)![]() 2NH3(g) ΔH<0可知反应物所含键能总和大于生成物所含键能总和
2NH3(g) ΔH<0可知反应物所含键能总和大于生成物所含键能总和
B.常温常压下,电解饱和食盐水时,每生成2.24LCl2,电路中转移0.2mol电子
C.室温下,稀释纯碱溶液时,溶液的pH减小
D.反应Na2O(s)+CO2(g)=Na2CO3(s)常温下可自发进行,该反应为吸热反应
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com