
【题目】(7分)锂锰电池的体积小,性能优良,是常用的一次电池。该电池反应原理如图所示,其中电解质LiClO4溶于混合有机溶剂中,Li+通过电解质迁移入MnO2晶格中,
生成LiMnO2。回答下列问题:

(1)外电路的电流方向是由_______极流向_______极。(填字母)
(2)电池正极反应式为________________________________________。
(3)是否可用水代替电池中的混合有机溶剂?_______(填“是”或“否”);
原因是____________________________________________________________。
 【答案】⑴ b a ⑵ MnO2+e—+Li+=LiMnO2 ⑶ 否;电极Li是活泼金属,能与水反应
【答案】⑴ b a ⑵ MnO2+e—+Li+=LiMnO2 ⑶ 否;电极Li是活泼金属,能与水反应
(电极反应式和原因各2分,其它每空1分,共7分)
【解析】
试题分析:(1)该电池中Li失去电子生成Li+,所以Li作电池的负极,则a是负极,b是正极,所以外电路中的电流方向由正极流向负极,所以从b流向a;
(2)正极发生还原反应,根据Li+通过电解质迁移入MnO2晶格中,生成LiMnO2。则MnO2得电子与锂离子生成LiMnO2,因此电解反应式为MnO2+e-+Li+=LiMnO2;
(3)不能用水代替电池中的混合有机溶剂,因为Li是活泼金属,与水反应,消耗Li,无法参与原电池反应,不能产生电流。


 期末宝典单元检测分类复习卷系列答案
期末宝典单元检测分类复习卷系列答案科目:高中化学 来源: 题型:
【题目】下列说法正确的是
A. 食用植物油属于人体所需的三大营养物质之一
B. 分馏、干馏都是物理变化,裂化、裂解都是化学变化
C. 淀粉、蛋白质、葡萄糖都是高分子化合物
D. 甲烷、汽油、生物柴油、酒精都是碳氢化合物,均可作为燃料
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学兴趣小组对某品牌牙膏中摩擦剂成分及其含量进行以下探究:
查得资料:该牙膏摩擦剂由碳酸钙、氢氧化铝组成;牙膏中其它成分遇到盐酸时无气体生成。
Ⅰ.摩擦剂中氢氧化铝的定性检验:
取适量牙膏样品,加水充分搅拌、过滤。
(1)往滤渣中加入过量NaOH溶液,过滤。氢氧化铝与NaOH溶液反应的离子方程式是 。
(2)往(1)所得滤液中先通入过量二氧化碳,再加入过量稀盐酸。观察到的现象是 。
Ⅱ.牙膏样品中碳酸钙的定量测定:
利用如图所示装置(图中夹持仪器略去)进行实验,充分反应后,测定C中生成的BaCO3沉淀质量,以确定碳酸钙的质量分数。

依据实验过程回答下列问题:
(3)实验过程中需持续缓缓通入空气,其作用除了可搅拌B、C中的反应物外,还有: 。
(4)C中反应生成BaCO3的化学方程式是 。
(5)下列各项措施中,不能提高测定准确度的是 (填标号)。
a.在加入盐酸之前,应排净装置内的CO2气体
b.滴加盐酸不宜过快
c.在A~B之间增添盛有浓硫酸的洗气装置
d.在B~C之间增添盛有饱和碳酸氢钠溶液的洗气装置
(6)实验中准确称取8.00g样品三份,进行三次测定,测得BaCO3平均质量为3.94g,则样品中碳酸钙的质量分数为 。
(7)有人认为不必测定C中生成的BaCO3质量,只要测定装置C在吸收CO2前后的质量差,一样可以确定碳酸钙的质量分数。实验证明按此方法测定的结果明显偏高,原因是 。
查看答案和解析>>
科目:高中化学 来源: 题型:
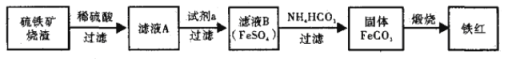
【题目】利用硫铁矿烧渣(主要成分为Fe2O3、FeO、SiO2等)制备铁红,大致生产过程如下:
请回答:
⑴检验滤液A 中含有Fe2+的方法是 。
⑵滤液A→B发生反应的离子方程式为 。
⑶在空气中煅烧FeCO3的方程式为 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】反应A(g)![]() B(g) +C(g)在容积为1.0L的密闭容器中进行,A的初始浓度为0.050mol/L。温度T1和T2下A的浓度与时间关系如图所示。回答下列问题:
B(g) +C(g)在容积为1.0L的密闭容器中进行,A的初始浓度为0.050mol/L。温度T1和T2下A的浓度与时间关系如图所示。回答下列问题:

(1)上述反应的温度T1 T2(填“大于”、“小于”或“等于”)
(2)若温度T2时,5min后反应达到平衡,A的转化率为70%, 则:
①平衡时体系总的物质的量为 。
②反应在0~5min区间的平均反应速率v(A)= 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据元素周期表和周期律分析下面推断错误的是
A. 铍原子失电子能力比镁弱
B. HI比砹的氢化物稳定
C. 氢氧化铝碱性比氢氧化镁强
D. 高氯酸的酸性比硫酸强
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是
A.含有共价键的化合物一定是共价化合物
B.阴、阳离子间通过静电引力而形成的化学键叫做离子键
C.NH3的稳定性很强,是因为其分子间能形成氢键
D.需要加热才能发生的反应不一定是吸热反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】2015年8月12日天津港特大爆炸事故,再一次引发了人们对环境问题的关注。据查危化仓库中存有大量的钠、钾、白磷(P4)、硝酸铵和氰化钠(NaCN)。爆炸事故中,因爆炸冲击导致氰化钠泄漏,可以通过喷洒双氧水或硫代硫酸钠溶液来处理,以减轻污染。
资料:氰化钠白色结晶颗粒、易潮解、有微弱的苦杏仁气味、剧毒、易溶于水、易水解生成氰化 氢、水溶液呈碱性。
(1)白磷有毒,能和氯酸溶液发生氧化还原反应:3P4 +10HC1O3 +18H2 O=10HC1+12H3 PO4,该反应的氧化产物是 ,若有1 mo1 P4参加反应转移电子为 mol。
(2)氰化钠(NaCN)是一种化工原料,用于基本化学合成、电镀、冶金和有机合成医药、农药及金属处理等方面。
①已知:25℃时,HCN的电离平衡常数Ka = 6.2×10-10,H2CO3在25℃时的电离平衡常数是Ka1=4.5×10-7 Ka2=4.7×10-11,则向NaCN溶液通入少量CO2反应方程式是: 。
②常温下,氰化钠能与过氧化氢溶液反应,生成碳酸氢钠和能使湿润的红色石蕊试纸变蓝色的气体,大大降低其毒性。该反应的化学方程式是: 。
(3)实验室通过如图所示装置制备Na2SO3。

装置a中盛装Na2SO3固体的仪器名称是 ;装置b的作用是 。
(3)装置c中的产物有Na2S2O3和CO2气体等,实验结束后,装置d中的溶质有NaOH、Na2CO3,还可能有 。
(4)实验结束后,在e处最好连接盛 (选填“NaOH溶液”、“水”、“CC14”中任一种。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com