
分析 燃烧热是1mol可燃物完全燃烧生成稳定氧化物时放出的热量,根据燃烧热的概念分别写出CO、甲醇燃烧的热化学方程式,然后利用盖斯定律写出甲醇不完全燃烧生成CO和液态水的热化学方程式.
解答 解:CO(g)和CH3OH(l)的燃烧热△H分别为-283.0kJ•mol-1和-726.5kJ•mol-1,则
氢气燃烧的热化学方程式为:①CO(g)+$\frac{1}{2}$O2(g)=CO2(g)△H=-283.0kJ•mol-1,
甲醇燃烧的热化学方程式为:②CH3OH(l)+$\frac{3}{2}$O2(g)=CO2(g)+2 H2O(l)△H=-726.5kJ•mol-1,
由盖斯定律可知,②-①可得甲醇不完全燃烧生成CO和液态水的热化学方程式:CH3OH(l)+O2(g)=CO(g)+2 H2O(l),△H=-726.5kJ•mol-1-(-283.0kJ•mol-1)=-443.5kJ•mol-1,
故答案为:CH3OH(l)+O2(g)=CO(g)+2 H2O(l)△H=-443.5kJ•mol-1.
点评 本题考查了热化学方程式的书写及盖斯定律的应用,题目难度不大,明确盖斯定律的内容为解答关键,注意掌握热化学方程式的书写原则,试题有利于提高学生的分析能力及灵活应用能力.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案科目:高中化学 来源: 题型:选择题
| A. | NH4Cl H2O CO2 | B. | NaCl MgCl2 Na2O | ||
| C. | H2O Na2O CO2 | D. | CaCl2 NaOH H2SO4 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | SiO2不能与HNO3、H2SO4等所有的酸反应 | |
| B. | 由Na2CO3+SiO$\frac{\underline{\;高温\;}}{\;}$Na2SiO3+CO2↑可知硅酸的酸性比碳酸的酸性强 | |
| C. | 硅胶常用于做干燥剂 | |
| D. | CO2与SiO2均是酸性氧化物,溶于水均得到相应的酸 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 苯(苯酚):氢氧化钠溶液,充分震荡静止后,分液 | |
| B. | 乙醇(水):加入新制生石灰,蒸馏 | |
| C. | 溴苯(溴):加入氢氧化钠溶液,充分震荡静止后,分液 | |
| D. | 乙酸(乙醇):加入金属钠,蒸馏 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
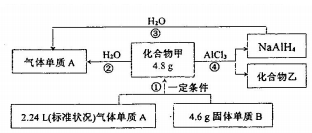
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:填空题
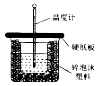 (1)在一定条件下N2与H2反应生成NH3,请回答:
(1)在一定条件下N2与H2反应生成NH3,请回答:查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 5.6gFe在氧气中燃烧,完全反应时转移电子数为0.3NA | |
| B. | 标准状况下,4.48L氦气中所含原子数为0.2NA | |
| C. | NA个Fe(OH)3胶体粒子的质量为107g | |
| D. | 带温下,l.7gNH3和3.65gHCl混合后,气体分子数为0.2NA |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com