
 2 SO3��Ӧ�������Ӻ�Ӧ�ﵽ��ѧƽ��״̬���������������ѹǿ��Ϊԭ����90% ����÷�Ӧ�ﵽƽ��ʱSO2��ת����Ϊ______________��
2 SO3��Ӧ�������Ӻ�Ӧ�ﵽ��ѧƽ��״̬���������������ѹǿ��Ϊԭ����90% ����÷�Ӧ�ﵽƽ��ʱSO2��ת����Ϊ______________�� ��У����ϵ�д�
��У����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A��a��b | B��ƽ��������Ӧ�����ƶ��� |
| C��A��ת���ʼ�С�� | D��B������������С�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
 CaMg2Al2Si3O12
CaMg2Al2Si3O12| A���Ƴ�ʯ���� | B��þ���ʯ���� |
| C���Ƴ�ʯ��þ���ʯ���� | D������þ��ʯ����ʯ���� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
 2HI(g)һ�����ڻ�ѧƽ��״̬����
2HI(g)һ�����ڻ�ѧƽ��״̬���� | A����λʱ������1mol H2���ģ�ͬʱ��1mol I2���� |
| B�������ڵ�ѹǿ���ֲ��� |
| C��H2(g����I2(g����HI(g)��Ũ����� |
| D����λʱ������1mol I-I������ͬʱ��2mol H��I���γ� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
 2C(g) ?H <0�����������������
2C(g) ?H <0�����������������| A�������¶�v��������v���棩������v���������ĸ��� |
| B����������ѹǿ���䣬���뺤����v��������v���棩����С |
| C������A��Ũ��v������������v���棩���С |
| D�����ô���һ��v��������v���棩ͬʱ����������ı�����ͬ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
 bB��������ƽ������¶Ȳ��䣬�������������1�������ﵽ��ƽ��ʱ��B��Ũ����ԭ����60%������˵����ȷ���ǣ�
bB��������ƽ������¶Ȳ��䣬�������������1�������ﵽ��ƽ��ʱ��B��Ũ����ԭ����60%������˵����ȷ���ǣ�| A��ƽ�����淴Ӧ�����ƶ��ˣ� | B������A��ת���ʼ����ˣ� |
| C������B���������������ˣ� | D��a>b�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ������
 CH3OH(g)��H2O(g) ��H����49.0kJ/mol
CH3OH(g)��H2O(g) ��H����49.0kJ/mol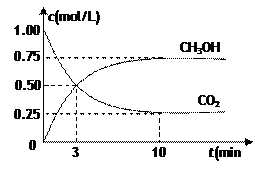

| A�������¶� | B������He(g)��ʹ��ϵѹǿ���� |
| C����H2O(g)����ϵ�з��� | D���ٳ���1mol CO2��3mol H2 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
 2NH3(g) DH����92.4kJ��mol��1���ڷ�Ӧ�����У�����Ӧ���ʵı仯��ͼ������˵����ȷ����
2NH3(g) DH����92.4kJ��mol��1���ڷ�Ӧ�����У�����Ӧ���ʵı仯��ͼ������˵����ȷ����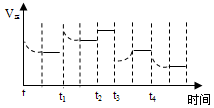
| A��t1ʱ�������¶� | B��t2ʱ������ѹǿ |
| C��t3ʱ��С��NH3��Ũ�� | D��t4ʱ�������¶� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A���÷�Ӧ��ƽ�ⳣ������ʽK��c(H2O)/c(H2) |
| B����������������ܶȻ�ѹǿ���ֲ��䣬��˵���÷�Ӧ�Ѵﵽƽ��״̬ |
| C����Na2SO4�������ı���ʼ����H2��Ũ�ȣ���ƽ��ʱH2��ת���ʲ��� |
| D������ʼʱͶ��2.84gNa2SO4��һ����H2����Ӧ��ƽ��ʱ�����ڹ��干��2.264g����Na2SO4��ת����Ϊ45% |
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com