
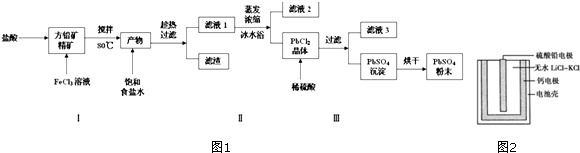
���� ��1���������������ΪPbCl2��S�����������ᡢ�Ȼ�����PbS����������ԭ��Ӧ��SԪ�ػ��ϼ����ߣ�����Ԫ�صĻ��ϼ۽��ͣ��ݴ�д����Ӧ�����ӷ���ʽ������Fe3+��Pb2+������������ʽ��ȫ����ʱ��Һ��pH�����жϣ�
��2�����ݼ��뱥��ʳ��ˮ����ڻ�ѧƽ�⣺PbCl2��s��+2Cl-��aq��?PbCl4-��aq����H��0�����ڱ�ˮԡ�У��¶Ƚϵͣ������¶ȶԻ�ѧƽ���Ӱ���ж�ʹ�ñ�ˮԡ��ԭ��
��3����֪��Ksp��PbSO4��=1.08��10-8��Ksp��PbCl2��=1.6��10-5��PbCl2����ת��ΪPbSO4��������ΪPbCl2�м���ϡ�����ƻ����Ȼ�Ǧ���ܽ�ƽ�⣬ʹ�ܽ�ƽ�������ƶ���������Ǧ��
��4����Һ2����Ҫ�ɷ���FeCl2����������ⷴӦ������FeCl3���ݴ�д����Ӧ�����ӷ���ʽ��
��5�����ݷŵ�ʱǦ���ع���ԭ��Ϊԭ��أ�����ԭ���ԭ�����������������ƶ����ɼ����ϼ۱仯д�������ĵ缫��Ӧʽ�����ݵ缫����ʽ������ؼ��㣮
��� �⣺��1�������������PbCl2��S�����������ᡢ�Ȼ�����PbS����������ԭ��Ӧ��SԪ�ػ��ϼ����ߣ�����Ԫ�صĻ��ϼ۽��ͣ���Ӧ�����ӷ���ʽΪ��PbS+2Fe3++2Cl-=PbCl2+2Fe2++S��Fe3+��Pb2+������������ʽ��ȫ����ʱ����Һ��PHֵ�ֱ�Ϊ3.2��7.04�����Լ����������һ��Ŀ����Ϊ�˿���PHֵ��0.5��1.0��ԭ��������Fe3+��Pb2+��ˮ�⣬
�ʴ�Ϊ��PbS+2Fe3++2Cl-=PbCl2+2Fe2++S������Fe3+��Pb2+��ˮ�⣻
��2�����뱥��ʳ��ˮ����ڻ�ѧƽ�⣺PbCl2��s��+2Cl-��aq��?PbCl4-��aq����H��0���ڱ�ˮԡ�У��¶Ƚϵͣ�ʹƽ�����������ƶ����Ӷ�����PbCl2�����������
�ʴ�Ϊ���ñ�ˮԡʹ��ӦPbCl2��s��+2Cl-��aq��?PbCl4-��aq�������ƶ���ʹPbCl4-����ת��ΪPbCl2�����������
��3������������Ϣ��֪��Ksp��PbSO4��=1.08��10-8��Ksp��PbCl2��=1.6��10-5����ϳ�����ת����PbCl2����ת��ΪPbSO4��������ΪPbCl2�м���ϡ�����ƻ����Ȼ�Ǧ���ܽ�ƽ�⣬ʹ�ܽ�ƽ�������ƶ���������Ǧ����Ӧ�����ӷ���ʽΪ��PbCl2��s��+SO42-��aq��?PbSO4 ��s��+2Cl-��aq����
�ʴ�Ϊ��PbCl2��s��+SO42-��aq��?PbSO4 ��s��+2Cl-��aq����
��4����Һ2����Ҫ�ɷ���FeCl2����������ⷴӦ������FeCl3��˫��ˮ������������Ӧ�����ӷ���ʽΪ��2Fe2++H2O2+2H+=2Fe3++2H2O��
�ʴ�Ϊ��2Fe2++H2O2+2H+=2Fe3++2H2O��
��5��Ǧ���طŵ�����У�Li+�������ƶ��������ϸ�ʧȥ���ӷ���������Ӧ���缫����ʽΪCa+2Cl--2e-�TCaCl2�������ܷ�ӦPbSO4+2LiCl+Ca�TCaCl2+Li2SO4+Pb������1molpbʱת��2mol���ӣ���ת��0.2mol����ʱ������0.1molǦ������Ϊ20.7gpb��
�ʴ�Ϊ��������Ca+2Cl--2e-�TCaCl2��20.7��
���� ����ͨ������Ǧ��ĩ���Ʊ��������������Ʊ�ʵ�鷽������Ʒ�������Ŀ�Ѷ��еȣ�ע�����ճ��������Ʊ�ʵ�鷽������Ʒ�������ȷ�����������Ʊ�����Ϊ���ؼ��������ֿ�����ѧ���ķ������������������Ӧ����ѧ֪ʶ��������



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
 ��
���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �٢ڢܢ� | B�� | �٢ۢݢ� | C�� | �٢ۢܢ� | D�� | �٢ڢۢ� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
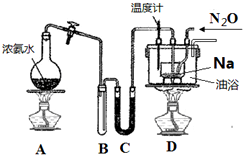 �������� ��NaN3�� ����Ϊ������ȫ���ҵ�ҩ���������������ˮ�������Ҵ������������ѣ�
�������� ��NaN3�� ����Ϊ������ȫ���ҵ�ҩ���������������ˮ�������Ҵ������������ѣ��鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ��ƶ���
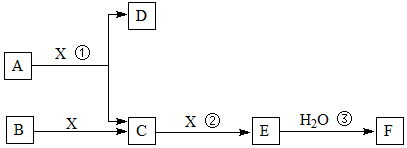
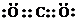 ��
���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 18O2-�ṹʾ��ͼ��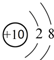 | |
| B�� | �������Ľṹ��ʽ�� | |
| C�� | NaHSO4����ʱ���뷽��ʽ��NaHSO4�TNa++HSO4- | |
| D�� | ģ�� �ɱ�ʾ������ӻ����Ȼ�̼���� �ɱ�ʾ������ӻ����Ȼ�̼���� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
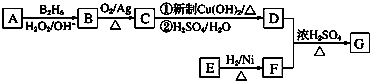
 ��
��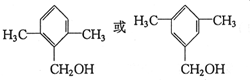 ��������һ�֣���
��������һ�֣���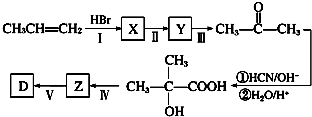
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �����ǿ��١�������ȷ�ⶨ��Է��������ķ��� | |
| B�� | ��������Dz������ڲⶨ������Ĺ����� | |
| C�� | �ú˴Ź���������1-������2-����� | |
| D�� | �������������ͬ���칹�� |
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com