
| A.同一周期元素的原子,半径越小越容易失去电子 |
| B.同一主族的元素,原子半径越大,氧化性越强 |
| C.ⅦA族元素形成的单质,其熔点随元素原子序数增大而降低 |
| D.从上到下,ⅦA族元素形成的氢化物稳定性逐渐减弱 |
 一本好题口算题卡系列答案
一本好题口算题卡系列答案科目:高中化学 来源:不详 题型:单选题
| A.原子半径:N>Z |
| B.单质的氧化性:Y>M |
| C.X、Z、M的氧化物均为共价化合物 |
| D.M、N的最高价氧化物对应的水化物均属于强酸 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
| 族 周期 | IA | | 0 | |||||
| 1 | ① | IIA | IIIA | ⅣA | VA | ⅥA | VIIA | |
| 2 | | | | | | ② | ③ | |
| 3 | ④ | ⑤ | | | | ⑥ | ⑦ | ⑧ |
| | 序号 | 条件 | 现象 | 结论 | |
| 温度/℃ | 催化剂 | ||||
| 第一组 | 1 | 40 | FeCl3溶液 | 快速产生大量气泡 | 相同条件下,温度升高,化学反应速率加快 |
| 2 | 20 | A | 缓慢产生适量气泡 | ||
| 3 | 5 | FeCl3溶液 | 缓慢产生极少量气泡 | ||
| 第二组 | 4 | t | MnO2 | 快速产生大量气泡 | |
| 5 | 20 | 无 | 缓慢产生极少量气泡 | ||
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.周期表的16族中,第ⅢB族所含的元素种类数最多 |
| B.在周期表中,元素的族序数都等于其原子的最外层电子数 |
| C.副族元素和第Ⅷ族元素都属于过渡金属 |
| D.第ⅦA族的砹(At),其单质为有色固体,AgAt不溶于水 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题

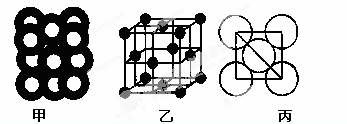
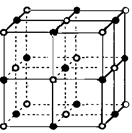
| 离子晶体 | NaCl | KCl | CaO |
| 晶格能/kJ·mol-1 | 786 | 715 | 3401 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.质子数相同,质量数不同,化学性质几乎相同 |
| B.质子数不同,质量数相同,化学性质相同 |
| C.质子数相同,中子数相同,化学性质几乎相同 |
| D.质子数相同,质量数不同,化学性质不同 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.在化合物中呈+2价 | B.单质与水反应放出氢气 |
| C.氢氧化物呈两性 | D.镭的还原性大于镁 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com