
 普通高中同步练习册系列答案
普通高中同步练习册系列答案 优翼小帮手同步口算系列答案
优翼小帮手同步口算系列答案科目:高中化学 来源:不详 题型:单选题
 2B(g)+C(g)(正反应为吸热反应)达平衡时,要使正反应速率降低,A的浓度增大,应采取的措施是 ( )
2B(g)+C(g)(正反应为吸热反应)达平衡时,要使正反应速率降低,A的浓度增大,应采取的措施是 ( )| A.加压 | B.使用催化剂 |
| C.减小C的浓度 | D.降温 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| 实验编号 | 1 | 2 | 3 | 4 | 5 |
| c(HI)/(mol·L-1) | 0.100 | 0.200 | 0.300 | 0.100 | 0.100 |
| c(H2O2)/(mol·L-1) | 0.100 | 0.100 | 0.100 | 0.200 | 0.300 |
| v/(mol·L-1·s-1) | 0.00760 | 0.0153 | 0.0227 | 0.0151 | 0.0228 |
| A.0.0380 mol·L-1·s-1 | B.0.152 mol·L-1·s-1 |
| C.0.608 mol·L-1·s-1 | D.0.760 mol·L-1·s-1 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.3.2mol | B.2.4mol | C.0.8mol | D.0.4mol |
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
| 试管编号 | 加3%Na2S2O3溶液/ml | 加H2O/ml | 加H2SO4(1:5)/滴 | 出现浑浊所用时间/s |
| ① | 3[ | 3 | 5 | a |
| ② | 4 | 2 | 5[] | b |
| ③ | 5 | 1 | 5 | c |
 [来源:
[来源:查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题

 。
。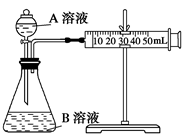
| 序号 | A溶液 | B溶液 |
| ① | 2 mL 0.1 mol/L H2C2O4溶液 | 4 mL 0.01 mol/L KMnO4溶液 |
| ② | 2 mL 0.2 mol/L H2C2O4溶液 | 4 mL 0.01 mol/L KMnO4溶液 |
| ③ | 2 mL 0.2 mol/L H2C2O4溶液 | 4 mL 0.01 mol/L KMnO4溶液和少量MnSO4 |
 mol/L
mol/L H2C2O4溶液,另取两支试管各加入4 mL 0.1 mol/L KMnO4溶液。将四支试管分成两组(各有一支盛有H2C2O4溶液和KMnO4溶液的试管),一组放入冷水中,另一组放入热水中,经过一段时间后,分别混合
H2C2O4溶液,另取两支试管各加入4 mL 0.1 mol/L KMnO4溶液。将四支试管分成两组(各有一支盛有H2C2O4溶液和KMnO4溶液的试管),一组放入冷水中,另一组放入热水中,经过一段时间后,分别混合 并振荡,记录溶液褪色所需时间。该实验目的是研究 对化学反应速率的影响,但该组同学始终没有看到溶液褪色,其原因是 。
并振荡,记录溶液褪色所需时间。该实验目的是研究 对化学反应速率的影响,但该组同学始终没有看到溶液褪色,其原因是 。查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
| A.使用高纯度的锌粒 | B.使用浓H2SO4 |
| C.使用小颗粒的锌粒 | D.使用浓HNO3 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
 2C,△H<0,下列条件的改变一定可以加快正反应速率的是
2C,△H<0,下列条件的改变一定可以加快正反应速率的是| A.增加压强 | B.升高温度 |
| C.增加A的量 | D.加入二氧化锰作催化剂 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com