
| A��ˮ���ӵĻ�ѧ���ʷ����˸ı� |
| B��ˮ�������������Ŀ���� |
| C��ˮ��������ˮ���Ӽ��������Ϊ���Ӽ������� |
| D��ˮ���ӵĽṹ���������ʷ����˸ı� |



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
46 22 |
47 22 |
48 22 |
49 22 |
50 22 |
| A��30 | B��28 | C��26 | D��24 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
 �ں�����������NaOH��Ӧ���������NaOH�����ʵ���Ϊ��������
�ں�����������NaOH��Ӧ���������NaOH�����ʵ���Ϊ��������| A��2mol | B��3mol |
| C��4mol | D��5mol |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A����ͳ�ϳɰ������ġ�H��0�����ͺϳɰ������ġ�H��0 |
| B�����ͺϳɰ�����������£����Ͻ��ܼ��ŵ��������� |
| C�����ʹ��������N2��H2��ת���� |
| D�����ַ����Ļ�ѧƽ�ⳣ����ͬ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��Na+ H+ NO3- Fe2+ |
| B��Ca2+ NO3- HCO3- OH- |
| C��K+ H+ Cl- SO42- |
| D��Fe3+ Cl- H+ CO32- |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��ϡ����������������ӦBa2++SO42-�TBaSO4�� |
| B����ˮ���Ȼ�����Һ��ӦAl3++3NH3?H2O�TAl��OH��3��+3NH4+ |
| C��������ϡ���ᷴӦFe+6H+�TFe3++3H2�� |
| D������ͨ��⻯����Һ��Cl2+I-�TCl-+I2 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
A�� 2��6-����-5-�һ����� |
B��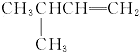 3-��-1-��ϩ |
C��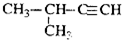 2-��-3-��Ȳ |
D�� 1��3��4-���ױ� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| ʱ��t/s | 0 | 50 | 150 | 250 | 350 |
| n��PCl3��/mol | 0 | 0.16 | 0.19 | 0.2 | 0.2 |
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com