
【题目】利用下列实验装置可以达到实验目的的是( )


A. 甲装置可以实现Cl2的制取、收集、尾气吸收
B. 乙装置可以实现乙酸乙酯的制取和收集
C. 丙装置可以形成Cu—Zn原电池
D. 丁装置可证明H2CO3的酸性大于H2SiO3
【答案】C
【解析】A、实验室可以采用KMnO4与浓盐酸在常温下反应制取Cl2,Cl2的密度大于空气的密度,采取向上排空气法收集Cl2,但集气瓶中的导气管应该长进短出,多余的Cl2可以用NaOH溶液吸收以防污染环境,A错误;B、加热条件下,乙醇和乙酸在浓硫酸的作用下发生酯化反应生成乙酸乙酯,收集乙酸乙酯时用饱和碳酸钠溶液吸收,乙酸乙酯中含有挥发出的乙酸和乙醇,乙酸和乙醇易溶于水,所以导气管不能伸入液面下,否则会引起倒流,B错误;丙装置中Zn比Cu活泼,Zn与Cu2+能发生自发的氧化还原反应,盐桥构成闭合回路,故可以形成Cu—Zn原电池,C正确;D、硝酸与碳酸钠反应产生的CO2气体与硅酸钠溶液反应生成白色沉淀H2SiO3,但硝酸是一种挥发性的酸,挥发出的硝酸也能与硅酸钠溶液反应产生白色沉淀H2SiO3,因此不能确定沉淀的生成是CO2引起的还是HNO3引起的,故无法证明H2CO3的酸性大于H2SiO3,本实验中如果用稀硫酸代替硝酸就可以证明H2CO3的酸性大于H2SiO3,D错误。正确答案为C。


 同步练习强化拓展系列答案
同步练习强化拓展系列答案科目:高中化学 来源: 题型:
【题目】下列选项中符合如图关系的是( ) 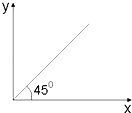
A.第二周期的核电荷数和最高化合价之间的关系
B.烷烃中碳原子数(X)与氢原子数(Y)的关系
C.温度大于100℃时,CH4和C2H4的混合气体在氧气中充分燃烧,同温同压下燃烧前后参与反应的气体的体积之和(X)与生成物的气体体积之和(Y)的关系
D.燃烧一定质量C2H4与C3H6的混合气体,消耗O2的物质的量(Y)与C3H6的质量分数(X)的关系
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用光洁的铂丝蘸取无色溶液在无色灯焰上灼烧时观察到黄色火焰,下列叙述正确的是( )
A.只含有Na+B.一定含Na+,也可含K+
C.既含Na+又含有K+D.可能含Na+或K+中一种
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】分析如图,不能得出的结论是( ) 
A.H2与O2反应是放热反应
B.断开化学键要放出能量
C.化学反应伴随着物质变化和能量变化
D.2mol H2和1mol O2具有的总能量高于2mol H2O 的总能量
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硫化锌(ZnS)是一种重要的化工原料,难溶于水,可由炼锌的废渣锌灰制取,其工艺流程如下图所示。
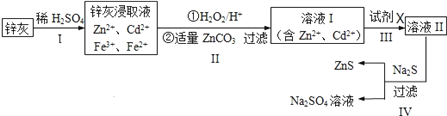
(1)为提高锌灰的浸取率,可采用的方法是____________(填序号)。
①研磨 ②多次浸取 ③升高温度 ④加压 ⑤搅拌
(2)步骤Ⅱ所得滤渣中的物质是_______________(写化学式)。
(3)步骤Ⅲ中可得Cd单质,为避免引入新的杂质,试剂X应为____________。
(4)步骤Ⅳ还可以回收Na2SO4来制取Na2S。
①检验ZnS固体是否洗涤干净的方法是_________________。
②Na2S可由等物质的量的Na2SO4和CH4在高温、催化剂条件下制取。化学反应方程式为_______________________________;
(5)若步骤Ⅱ加入的ZnCO3为bmol,步骤Ⅲ所得Cd为dmol,最后得到VL、物质的量浓度为cmol/L的Na2SO4溶液。则理论上所用锌灰中含有锌元素的质量为____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、D是由常见的短周期非金属元素形成的单质,常温下A是淡黄色粉末,B、D是气体,F、G、H的焰色反应均为黄色,水溶液均显碱性,E有漂白性。它们之间的转化关系如图所示(部分产物及反应条件已略去),回答下列问题:
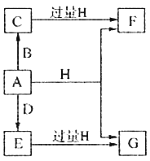
(1)A所含元素在周期表中的位置为______________,C的电子式为_______________。
(2)A与H在加热条件下反应的化学方程式为__________________。
(3)将A溶于沸腾的G溶液中可以制得化合物I,I在酸性溶液中不稳定,易生成等物质的量的A和E,I在酸性条件下生成A和E的离子方程式为____________________。I是中强还原剂,在纺织、造纸工业中作为脱氯剂,向I溶液中通入氯气可发生反应,参加反应的I和氯气的物质的量比为1:4,该反应的离子方程式为__________________。
(4)向含有0.4molF、0.1molG的混合溶液中加入过量盐酸,完全反应后收集到aL气体C(标准状况),取反应后澄清溶液,加入过量FeCl3溶液,得到沉淀3.2g,则a=____________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】二氧化氯(ClO2)是极易溶于水且不与水发生化学反应的黄绿色气体,沸点为 11℃,可用于处理含硫废水。某小组在实验室中探究 ClO2 与 Na2S 的反应。回答下列问题:
(1)ClO2 的制备
已知:SO2+2NaClO3+H2SO4=2ClO2↑+2NaHSO4
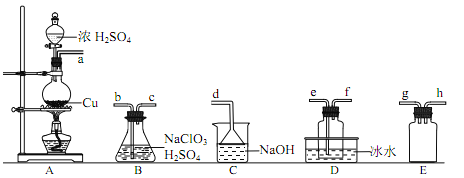
①装置 A 中反应的化学方程式为____________。
②欲收集干燥的 ClO2,选择上图中的装置,其连接顺序为 a→________________(按气流方向,用小写字母表示)
③装置 D 的作用是__________________。
(2)ClO2 与 Na2S 的反应
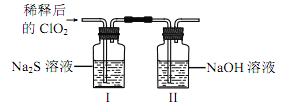
将上述收集到的 ClO2 用 N2 稀释以增强其稳定性,并将适量的稀释后的 ClO2 通入上图所示装置中充分反应,得到无色澄清溶液。一段时间后,通过下列实验探究 I 中反应的产物。
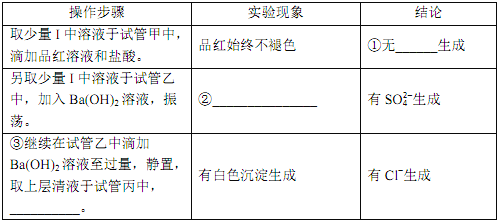
①___________。②___________。③___________。
④ClO2 与 Na2S 反应的离子方程式为____________。用于处理含硫废水时,ClO2 相对于Cl2 的优点是____________(任写一条)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用NA表示阿伏伽德罗常数的值.下列判断正确的是( )
A.常温常压下,16 g O3所含的氧原子数目为NA
B.1 molL﹣1CaCl2溶液中含有的Cl﹣数目为2NA
C.5.6 g Fe与足量盐酸反应失去的电子数目为0.3NA
D.标准状况下,22.4 L苯含有的分子数目为NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将0.02mol铜片溶于100mL9mol/LHNO3中,产生336mL气体(只含NO、NO2)。该气体与一定量O2混合后用水恰好完全吸收,则通入的O2体积为(气体体积均为标准状况)( )
A. 22.4mL B. 33.6mL
C. 44.8mL D. 224mL
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com