
【题目】SO2是一种重要的化工原料,也是一种环境污染物。
(1)SO2可用于工业制Br2过程中吸收潮湿空气中的Br2,反应的离子方程式是_____________________________。
(2)直接排放含SO2的烟气会形成酸雨,危害环境。用化学方程式表示SO2形成硫酸型酸雨的反应____________________________。
(3)工业上用Na2SO3溶液吸收烟气中的SO2。
将烟气通入1.0 mol·L-1的Na2SO3溶液,溶液pH不断减小。当溶液pH约为6时,吸收SO2的能力显著下降,应更换吸收剂。
①此时溶液中c(SO![]() )的浓度是0.2 mol·L-1,则溶液中c(HSO
)的浓度是0.2 mol·L-1,则溶液中c(HSO![]() )是________mol·L-1,由此说明NaHSO3溶液显________性,用化学平衡原理解释:_____________________________。
)是________mol·L-1,由此说明NaHSO3溶液显________性,用化学平衡原理解释:_____________________________。
②向pH约为6的吸收剂中通入足量的O2,可将其中的NaHSO3转化为两种物质,反应的化学方程式是___________________________________。
【答案】(1)SO2+Br2+2H2O===SO![]() +2Br-+4H+
+2Br-+4H+
(2)SO2+H2O![]() H2SO3;2H2SO3+O2===2H2SO4
H2SO3;2H2SO3+O2===2H2SO4
(3)①1.6 酸 NaHSO3溶液中存在HSO![]()
![]() H++SO
H++SO![]() 和 HSO
和 HSO![]() +H2OH2SO3+OH-,HSO
+H2OH2SO3+OH-,HSO![]() 的电离程度大于其水解程度 ②2NaHSO3+O2===Na2SO4+H2SO4
的电离程度大于其水解程度 ②2NaHSO3+O2===Na2SO4+H2SO4
【解析】(1) SO2可以被Br2氧化为H2SO4,Br2被还原为HBr,两者均为强酸,写离子方程式时均可拆成离子形式。(2)在空气中SO2和水生成H2SO3,H2SO3易被空气中的氧气氧化为H2SO4。(3)①发生的反应为:Na2SO3+SO2+H2O===2NaHSO3,剩余SO![]() 为0.2 mol·L-1,说明反应的SO
为0.2 mol·L-1,说明反应的SO![]() 为0.8 mol·L-1,则生成的HSO
为0.8 mol·L-1,则生成的HSO![]() 的浓度为1.6 mol·L-1。由题给信息,“溶液pH约为6时,吸收SO2的能力显著下降”可判断NaHSO3溶液呈酸性。HSO
的浓度为1.6 mol·L-1。由题给信息,“溶液pH约为6时,吸收SO2的能力显著下降”可判断NaHSO3溶液呈酸性。HSO![]() 在溶液中既可以电离(HSO
在溶液中既可以电离(HSO![]() H++SO
H++SO![]() )又可以水解(HSO
)又可以水解(HSO![]() +H2O
+H2O![]() H2SO3+OH-),溶液呈酸性,说明电离程度大于水解程度。②+4价的硫有较强的还原性,能被O2氧化为SO
H2SO3+OH-),溶液呈酸性,说明电离程度大于水解程度。②+4价的硫有较强的还原性,能被O2氧化为SO![]() ,因此可生成H2SO4和Na2SO4两种物质。
,因此可生成H2SO4和Na2SO4两种物质。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A.BaSO4难溶于水,BaSO4属于非电解质
B.非电解质的水溶液一定不导电
C.电解质主要包括:酸、碱、盐和部分氧化物
D.电解质在任何情况下均一定导电
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关物质的性质与用途具有对应关系的是( )
A.SO2具有氧化性,可用于漂白纸浆
B.NH4HCO3受热易分解,可用作氮肥
C.Fe2(SO4)3易溶于水,可用作净水剂
D.Al2O3熔点高,可用作耐高温材料
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】据报道,在300 ℃、70 MPa下由二氧化碳和氢气合成乙醇已成为现实。2CO2(g)+6H2(g) ![]() CH3CH2OH(g)+3H2O(g)下列叙述不正确的是
CH3CH2OH(g)+3H2O(g)下列叙述不正确的是
A.使用CuZnFe催化剂可大大提高生产效率
B.恒容时,充入大量CO2气体可提高H2的转化率
C.反应需在300 ℃时进行可推测该反应是吸热反应
D.从平衡混合气体中及时分离出CH3CH2OH和H2O可提高CO2和H2的利用率
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C、D、E代表前四周期原子序数依次增大的五种元素。A、D同主族且有两种常见化合物DA2和DA3;工业上电解熔融C2A3制取单质C;B、E除最外层均只有2个电子外,其余各层全充满,E位于元素周期表的ds区。回答下列问题:
(1)B、C中第一电离能较大的是_________,基态D原子价电子的轨道表达式为____________。
(2)DA2分子的VSEPR模型是____________。H2A比H2D熔沸点高得多的原因是____________。
(3)实验测得C与氯元素形成化合物的实际组成为C2Cl6,其球棍模型如图所示。已知C2Cl6 在加热时易升华,与过量的NaOH溶液反应可生成Na[C(OH)4]。
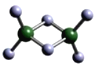
① C2Cl6属于____________晶体(填晶体类型),其中C原子的杂化轨道类型为____________杂化。
② [C(OH)4]-中存在的化学键有___________。
(4)工业上制备B的单质是电解熔融B的氯化物,而不是电解BA,原因是_____________。
(5)B、C的氟化物晶格能分别是2957 kJ·mol-1、5492 kJ·mol-1,二者相差很大的原因是____________。
(6)D与E所形成化合物晶体的晶胞如图所示。
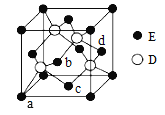
① 在该晶胞中,E的配位数为______________。
② 已知该晶胞的密度为ρ g/cm3,则其中两个D原子之间的距离为_________ pm(列出计算式即可)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】我国科技创新成果斐然,下列成果中获得诺贝尔奖的是( )
A.徐光宪建立稀土串级萃取理论
B.屠呦呦发现抗疟新药青蒿素
C.闵恩泽研发重油裂解催化剂
D.侯德榜联合制碱法
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】汽车尾气中含有上百种不同的化合物,其中的污染物有固体悬浮颗粒、一氧化碳、二氧化碳、碳氢化合物、氮氧化合物、铅及硫氧化合物等,一辆轿车一年排放的有害废气比自身重量大3倍。其中NO气体是由于内燃机燃烧的高温引起N2和O2反应所致:N2(g)+O2(g)![]() 2NO(g) △H>0,已知该反应在2404℃时,平衡常数K=64×10-4。请回答:
2NO(g) △H>0,已知该反应在2404℃时,平衡常数K=64×10-4。请回答:
(1)某温度下,向4L密闭容器中充入N2和O2各4mol,平衡时,5分钟后O2的物质的量为1mol,则N2的反应速率是____________。
(2)恒容条件下,判断该反应达到平衡的标志是________。(填字母序号)。
A.消耗1mol N2同时生成1mol O2 B.混合气体密度不变
C.混合气体平均相对分子质量不变 D.2v(N2)正=v(NO)逆
(3)将N2、O2的混合气体充入恒温恒容密闭容器中,下列变化趋势正确的是________(填字母序号)。

(4)可逆反应N2(g)+O2(g)![]() 2NO(g)的平衡常数表达式为____________。温度升高,平衡常数将会
2NO(g)的平衡常数表达式为____________。温度升高,平衡常数将会
_____________(填“增大、或“减小”)
(5)该温度下,某时刻测得容器内N2、O2、NO的浓度分别为2.5×10-1mol·L-1、4.0×10-2mol·L-1和3.0×10-3mol·L-1,此时反应___________(填“处于化学平衡状态”、“向正反应方向进行”或“向逆反应方向进行”)。
(6) 火箭燃料N2H4(肼)在NO2中燃烧,生成N2、液态水。已知:
N2(g)+2O2(g)=2NO2(g) △H1=+67kJ/mol
N2H4(g)+O2(g)=N2(g)+2H2O(l) △H2=-534kJ/mol
由此请写出发射火箭时燃烧反应的热化学方程式____________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com