
下列解释实际应用的原理表达式中,不正确的是
A. 用排饱和食盐水法收集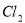 :
: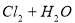

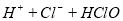
B. 热的纯碱溶液碱性增强: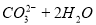

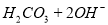
C. 向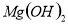 悬浊液中加入
悬浊液中加入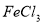 溶液:
溶液: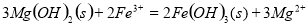
D. 配制FeCl3溶液时为防止溶液浑浊常加入少量稀盐酸Fe3++3H2O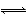 Fe(OH)3+3H+,
Fe(OH)3+3H+,
B
【解析】
试题分析:A. 用排饱和食盐水法收集Cl2,是因为在水中存在可逆反应,Cl2+H2O H++Cl-+HClO,当水中存在Cl-平衡逆向移动,可以减少Cl2的溶解,因此可以用排饱和食盐水的方法收集,正确;B.Na2CO3是强碱弱酸盐水解使溶液显碱性,而盐水解的反应是吸热反应,所以升高温度,盐水解程度增大,溶液的碱性增强,但是盐水解是逐步进行的,因此该表达式错误;C.在Mg(OH)2的悬浊液中存在沉淀溶解平衡,当向该悬浊液中加 入FeCl3溶液时,由于在溶液中c(Fe3+)c3(OH-)>Ksp(Fe(OH)3),所以会形成氢氧化铁沉淀,会发生沉淀转化,正确; D. 配制FeCl3溶液时由于Fe3+水解产生氢氧化铁而使溶液浑浊,所以为抑制水解,防止溶液浑浊常加入少量稀盐酸,正确。
H++Cl-+HClO,当水中存在Cl-平衡逆向移动,可以减少Cl2的溶解,因此可以用排饱和食盐水的方法收集,正确;B.Na2CO3是强碱弱酸盐水解使溶液显碱性,而盐水解的反应是吸热反应,所以升高温度,盐水解程度增大,溶液的碱性增强,但是盐水解是逐步进行的,因此该表达式错误;C.在Mg(OH)2的悬浊液中存在沉淀溶解平衡,当向该悬浊液中加 入FeCl3溶液时,由于在溶液中c(Fe3+)c3(OH-)>Ksp(Fe(OH)3),所以会形成氢氧化铁沉淀,会发生沉淀转化,正确; D. 配制FeCl3溶液时由于Fe3+水解产生氢氧化铁而使溶液浑浊,所以为抑制水解,防止溶液浑浊常加入少量稀盐酸,正确。
考点:考查平衡原理的应用的知识。


科目:高中化学 来源:2014年全国普通高等学校招生统一考试理科综合能力化学(全国大纲卷解析版) 题型:实验题
(15 分)
苯乙酸铜是合成优良催化剂、传感材料——纳米氧化铜的重要前驱体之一。下面是它的一种实验室合成路线:
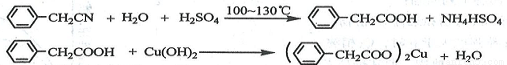
制备苯乙酸的装置示意图如下(加热和夹持装置等略):
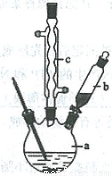
已知:苯乙酸的熔点为76.5 ℃,微溶于冷水,溶于乙醇。
回答下列问题:
(1)在250 mL三口瓶a中加入70 mL70%硫酸。配制此硫酸时,加入蒸馏水与浓硫酸的先后顺序是
。
(2)将a中的溶液加热至100 ℃,缓缓滴加40 g苯乙腈到硫酸溶液中,然后升温至130 ℃继续反应。在装置中,仪器b的作用是 ;仪器c的名称是 ,其作用是 。
反应结束后加适量冷水,再分离出苯乙酸粗品。加人冷水的目的是 。下列仪器中可用于分离苯乙酸粗品的是 (填标号)。
A.分液漏斗B.漏斗C.烧杯D.直形冷凝管E.玻璃棒
(3)提纯粗苯乙酸的方法是 ,最终得到44 g纯品,则苯乙酸的产率是 。
(4)用CuCl2? 2H2O和NaOH溶液制备适量Cu(OH)2沉淀,并多次用蒸馏水洗涤沉淀,判断沉淀洗干净的实验操作和现象是 。
(5)将苯乙酸加人到乙醇与水的混合溶剂中,充分溶解后,加入Cu(OH)2搅拌30min,过滤,滤液静置一段时间,析出苯乙酸铜晶体,混合溶剂中乙醇的作用是 。
查看答案和解析>>
科目:高中化学 来源:2013年普通高等学校招生全国统一考试化学(广东卷解析版) 题型:简答题
(16分)大气中的部分碘源于O3对海水中I-的氧化。将O3持续通入NaI溶液中进行模拟研究。
(1)O3将I-氧化成I2的过程由3步反应组成:
①I-(aq)+ O3(g)==IO-(aq)+O2(g) △H1
②IO-(aq)+H+(aq)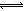 HOI(aq) △H2
HOI(aq) △H2
③HOI(aq)+ I-(aq)+ H+(aq)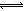 I2(aq)+H2O(l) △H3
I2(aq)+H2O(l) △H3
总反应的化学方程式为______,其反应△H=______。
(2)在溶液中存在化学平衡:I2(aq)+I-(aq)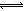 I3-(aq),其平衡常数表达式为_______。
I3-(aq),其平衡常数表达式为_______。
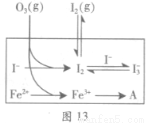
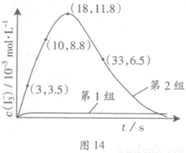
(3)为探究Fe2+对氧化I-反应的影响(反应体系如图13),某研究小组测定两组实验中I3-浓度和体系pH,结果见图14和下表。
编号 | 反应物 | 反应前pH | 反应后pH |
第1组 | O3+ I- | 5.2 | 11.0 |
第2组 | O3+ I-+ Fe2+ | 5.2 | 4.1 |
①第1组实验中,导致反应后pH升高的原因是_______。
②图13中的A为 。由Fe3+生成A的过程能显著提高I-的转化率,原因是_______。
③第2组实验进行18s后,I3-下降。导致下降的直接原因有(双选)______。
A.c(H+)减小 B.c(I-)减小 C.I2(g)不断生成 D.c(Fe3+)增加
(4)据图14,计算3~18s内第2组实验中生成I3-的平均反应速率(写出计算过程,结果保留两位有效数字)。
查看答案和解析>>
科目:高中化学 来源:2013-2014河南省原名校高三高考仿真模拟统一考试理综化学试卷(解析版) 题型:选择题
某有机物的分子式为C9H9ClO2 ,分子中含有1个苯环,苯环上有两个取代基,并能与NaHCO3溶液反应的同分异构体的数目为(不考虑立体异掏)
A.12种 B. 15种 C.18种 D. 21种
查看答案和解析>>
科目:高中化学 来源:2013-2014北京市房山区下学期高二期末测验化学试卷(解析版) 题型:填空题
(7分)某同学模拟工业“折点加氯法”处理氨氮废水的原理,进行如下研究。
装置(气密性良好,试剂已添加) | 操作 | 现象 |
| 打开分液漏斗活塞,逐滴加入浓氨水 | ⅰ.C中气体颜色变浅 ⅱ.稍后,C中出现白烟并逐渐增多 |
(1)浓氨水分解可以制氨气,写出A中反应的化学方程式是 。从平衡移动 的角度分析NaOH固体在氨水分解中的作用 。
(2)现象ⅰ,C中发生的反应为:2NH3(g)+3Cl2(g)= N2(g)+6HCl(g) ?H= —456 kJ·mol-1
已知: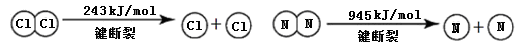
①NH3的电子式是 。
②断开1mol H-N键与断开1molH-Cl键所需能量相差约为 ,
(3)现象ⅱ中产生白烟的化学方程式是 。
(4)为避免生成白烟,该学生设计了下图装置以完成Cl2和NH3的反应。

若该装置能实现设计目标,则①石墨b电极上发生的是 反应(填“氧化”或“还原”)
②写出石墨a电极的电极反应式: 。
查看答案和解析>>
科目:高中化学 来源:2013-2014北京市房山区下学期高二期末测验化学试卷(解析版) 题型:选择题
下列叙述中,正确的是
A.用惰性电极电解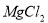 溶液分别得到单质
溶液分别得到单质 和Cl2
和Cl2
B.常温下,某溶液中由水电离出的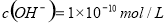 ,该溶液一定呈酸性
,该溶液一定呈酸性
C.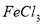 溶液和
溶液和 溶液加热蒸干、灼烧都得到
溶液加热蒸干、灼烧都得到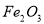
D.在AgBr饱和溶液中加入AgNO3溶液,达到平衡时,溶液中Br-浓度降低
查看答案和解析>>
科目:高中化学 来源:2013-2014北京市房山区下学期高二期末测验化学试卷(解析版) 题型:选择题
下列说法正确的是
A.某温度时, 1LpH=6的水溶液,含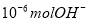 离子
离子
B.含10.6gNa2CO3溶液中,所含阴离子总数等于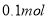
C.VLamol/LFeCl3溶液中,若Fe3+离子数目为1mol,则Cl-离子数目大于3mol。
D.电解精炼粗铜时,每转移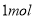 电子,阳极上溶解的
电子,阳极上溶解的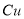 原子数必为
原子数必为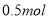
查看答案和解析>>
科目:高中化学 来源:2014秋季江西省赣州市十二县高一上学期期中联考化学试卷(解析版) 题型:选择题
浓H2SO4和木炭在加热时发生反应的化学方程式是:2H2SO4(浓)+C=CO2↑+2H2O+2SO2↑,则12g木炭和足量的浓硫酸反应后生成的气体在标况下的体积为
A.22.4L B.44.8L C.67.2L D.89.6L
查看答案和解析>>
科目:高中化学 来源:2014秋北京市高一上学期期中化学试卷(解析版) 题型:选择题
下列各组混合物不能用分液漏斗分离的是
A.四氯化碳和碘 B.花生油和水
C.四氯化碳和水 D.水和汽油
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com