
| A、水电离出来的c(OH-)=1.0×10-13mol?L-1 |
| B、该溶液的pH<13 |
| C、溶液中离子浓度关系:c(Na+)>c(CH3COO-)>c(OH-)>c(H+) |
| D、加入等浓度等体积的盐酸,溶液中:c(CH3COOH)+c(CH3COO-)=c(Cl-)+c(Na+) |


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
| A、乙醇、乙烷和乙酸都可以与钠反应生成氢气 |
| B、苯、乙醇和乙酸都能发生取代反应 |
| C、乙醇和乙酸都存在碳氧双键 |
| D、石油分馏可获得乙酸、苯及其同系物 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、K+、Fe3+、CO32-、NO3- |
| B、H+、K+、MnO4-、Cl- |
| C、Ba2+、Na+、HCO3-、OH- |
| D、K+、Na+、SO42-、S2- |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、△H1>0,△H2>0 |
| B、△H3>0,△H4>0 |
| C、△H2=△H4+△H5 |
| D、△H3=△H1-2△H2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、35Cl2与37Cl2互为同位素 |
B、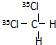 和 和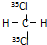 互为同分异构体 互为同分异构体 |
| C、与37Cl的得电子能力相同 |
| D、35Cl-和与它核外电子排布相同的微粒化学性质相同 |
查看答案和解析>>
科目:高中化学 来源: 题型:
A、 所示装置,蒸干NH4Cl饱和溶液制备NH4Cl晶体 |
B、 所示的气流方向可用于收集H2、NH3等 |
C、 所示装置,分离CCl4萃取I2水后的有机层和水层 |
D、 所示装置,可以证明氧化性:Cl2>Br2>I2 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com