
A.过氧化钠固体与水反应:2O22—+2H2O 4OH-+O2↑ 4OH-+O2↑ |
B.向明矾[KAl(SO4)2]溶液中逐滴加入Ba(OH)2溶液至SO42—恰好沉淀完全:2Al3++3SO42—+3Ba2++6OH- 2Al(OH)3↓+3BaSO4↓ 2Al(OH)3↓+3BaSO4↓ |
C.向次氯酸钠溶液中通入少量SO2:ClO-+SO2+H2O Cl-+SO42—+2H+ Cl-+SO42—+2H+ |
D.FeSO4酸性溶液暴露在空气中:4Fe2++O2+4H+ 4Fe3++2H2O 4Fe3++2H2O |
科目:高中化学 来源:不详 题型:填空题
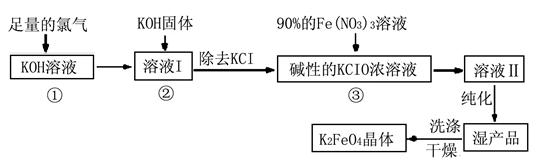
| A.为下一步反应提供碱性的环境 |
| B.使KClO3转化为KClO |
| C.与溶液I中过量的Cl2继续反应,生成更多的KClO |
| D.KOH固体溶解会放出较多的热量,有利于提高反应速率和KClO的纯度 |
 3Zn+2K2FeO4+8H2O,
3Zn+2K2FeO4+8H2O,查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
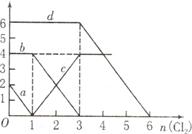
| A.d曲线代表溶液中Br—变化情况 |
| B.原溶液中FeI2的物质的量为2mol |
| C.原溶液中n(Fe2+):n(Br—)=2:3 |
| D.当通入2mol Cl2时,溶液中离子反应为:2Fe2++2I—+2Cl2=2Fe3++I2+4Cl— |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.澄清石灰水与过量的小苏打溶液反应:Ca2++OH-+HCO3-=CaCO3↓+H2O |
| B.明矾溶液中滴加Ba(OH)2溶液至SO42–恰好完全沉淀:Al3++Ba2++ SO42–+3OH–=BaSO4↓+Al(OH)3↓ |
| C.200 mL 2 mol·L–1的FeBr2溶液中通入11.2 L标准状况下的氯气:4 Fe2++6Br–+5Cl2=4Fe3++3Br2+ 10Cl– |
| D.在强碱溶液中次氯酸钠与Fe(OH)3反应生成Na2FeO4:3ClO–+2Fe(OH)3=2FeO42–+3Cl–+H2O+4H+ |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.利用醋酸溶解含碳酸钙的水垢:CaCO3+2H+=Ca2++H2O+CO2↑ |
B.用铜为电极电解饱和食盐水:2Cl-+2H2O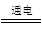 Cl2↑+H2↑+2OH- Cl2↑+H2↑+2OH- |
| C.在明矾溶液中滴加过量氨水:Al3++4NH3·H2O=AlO2—+4NH4++2H2O |
| D.在小苏打溶液中加少量Ba(OH)2溶液:2HCO3—+Ba2++2OH-=BaCO3↓+2H2O+CO32— |
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
 KI3
KI3| A.Na2S2O3 | B.AlCl3 | C.Na2CO3 | D.NaNO2 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题

查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题

| A.含0.01 mol KOH和0.01 mol Ca(OH)2的混合溶液中缓慢通入CO2 |
| B.NaHSO4溶液中逐滴加入Ba(OH)2溶液 |
| C.KAl(SO4)2溶液中逐滴加入Ba(OH)2溶液 |
| D.向含有少量氢氧化钠的偏铝酸钠溶液中滴加盐酸 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com