
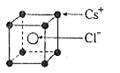
A.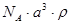 | B. | C.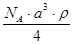 | D.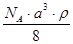 |
科目:高中化学 来源:不详 题型:单选题
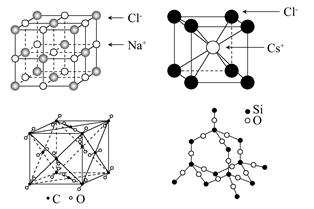
| A.同一主族的元素与另一相同元素所形成的化学式相似的物质不一定具有相同的晶体结构 |
| B.氯化钠、氯化铯和二氧化碳的晶体都有立方的晶胞结构,它们具有相似的物理性质 |
| C.二氧化碳晶体是分子晶体,其中不仅存在分子间作用力,而且也存在共价键 |
| D.在二氧化硅晶体中,平均每个Si原子形成4个Si-O共价单键 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.A1型密堆积是最密堆积,A3型密堆积不是最密堆积 |
| B.两者都是最密堆积,其中A3型密堆积是一、三、五……各层球心重合,二、四、六……各层球心重合;A1型密堆积是四、五、六各层球心分别和一、二、三各层球心重合 |
| C.原子晶体一般都采用A1型密堆积或A3型密堆积 |
| D.只有金属晶体才可能采用A1型密堆积或A3型密堆积 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
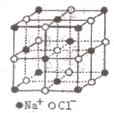
| A.一个金刚石的晶胞中有8个C原子 |
| B.金刚石的密度为3.54g·cm-1 |
| C.在该种CO2晶体中,一个CO2分子由一个C原子和二个氧原子构成 |
| D.在该种CO2晶胞中含氧原子8个 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.AlON和石英的化学键类型相同 |
| B.AlON和石英晶体类型相同 |
| C.AlON和(工业上通过电解法制备铝用的)Al2O3的化学键类型不同 |
| D.AlON和(工业上通过电解法制备铝用的)Al2O3晶体类型相同 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
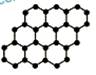
| A.石墨烯是一种有机化合物 |
| B.0.0012kg石墨烯中含有0.6mol质子 |
| C.不用其它试剂,利用丁达尔现象即可区分石墨和石墨烯 |
| D.剥离石墨属于物理变化过程 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.熔点2 700 ℃,导电性好,延展性强 |
| B.无色晶体,熔点3 500 ℃,不导电,质硬,难溶于水和有机溶剂 |
| C.无色晶体,能溶于水,质硬而脆,熔点800 ℃,熔化时能导电 |
| D.熔点-56.6 ℃,微溶于水,硬度小,固态或液态时不导电 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
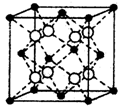
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com