
在两个恒容容器中有平衡体系:A(g) 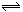 2B(g)和2C(g)
2B(g)和2C(g) 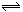 D(g),X1和X2分别是A和C的转化率。在温度不变情况下,均增加相同的A和C的物质的量,下列判断正确的是: ( )
D(g),X1和X2分别是A和C的转化率。在温度不变情况下,均增加相同的A和C的物质的量,下列判断正确的是: ( )
A.X1降低,X2增大 B.X1、X2均降低 C.X1增大,X2降低 D.X1、X2均增大
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
下列各组离子在指定条件下能大量共存的是
①漂白粉的水溶液中:Fe2+、Cl—、Ca2+、Na+ ②滴加石蕊试液呈红色的溶液:K+、NH4+、Cl—、S2— ③能够与金属Cu常温下反应放出气体的溶液:Fe3+、Al3+、SO42-、K+ ④常温下pH =2的溶液中:NH4+、Na+、Cl—、Cu2+ ⑤无色溶液中:K+、CH3COO—、HCO3—、MnO4—
A、②③ B、①③ C、③④ D、①⑤
查看答案和解析>>
科目:高中化学 来源: 题型:
下列有关物质分类或归纳正确的是( )
①电解质:明矾、冰醋酸、氯化银、纯碱 ②同素异形体:金刚石、石墨;C60、C70
③混合物:盐酸、漂白粉、水玻璃、水银 ④化合物:BaCl2、Ca(OH)2、HNO3、HT
A.①② B.②③ C.③④ D.②④
查看答案和解析>>
科目:高中化学 来源: 题型:
已知:C(s,金刚石)=C(s,石墨)△H=-1.9KJ/mol
C(s,金刚石)+O2(g)=CO2(g) △H1
C(s,石墨)+O2(g)=CO2(g) △H2
根据已述反应所得出的结论正确的是( )
A、△H1=△H2 B、△H1>△H2 C、△H1<△H2 D、金刚石比石墨稳定
查看答案和解析>>
科目:高中化学 来源: 题型:
可逆反应a A(s)+b B(g)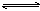 c C(g)+d D(g),反应过程中,当其它条件不变时,C的百分
c C(g)+d D(g),反应过程中,当其它条件不变时,C的百分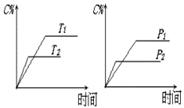 含量(C%)与温度(T)和压强(P)的关系如下图下列叙述正确的是
含量(C%)与温度(T)和压强(P)的关系如下图下列叙述正确的是
A、达平衡后,加入催化剂则C%增大
B、达平衡后,若升温,平衡左移
C、化学方程式中b >c +d
D、达平衡后,增加A的量有利于平衡向右移动
查看答案和解析>>
科目:高中化学 来源: 题型:
在一定温度和一定压强的容器中充入4升N2和H2的混合气体,反应达到平衡后,恢复到原温度,体积变为3.4升,容器内气体对相同条件下H2的相对密度为5.
计算:反应达到平衡时V(NH3)= 升,反应前
V(N2):V(H2)= ,N2的转化率为
 |
查看答案和解析>>
科目:高中化学 来源: 题型:
下列关于物质分类的正确组合是( )
| 分类 组合 | 碱 | 酸 | 盐 | 碱性 氧化物 | 酸性 氧化物 |
| A | Na2CO3 | H2SO4 | NaHCO3 | SiO2 | CO2 |
| B | NaOH | HCl | NaCl | Na2O | CO |
| C | NaOH | CH3COOH | CaF2 | SO3 | SO2 |
| D | KOH | HNO3 | CaCO3 | CaO | SO3 |
查看答案和解析>>
科目:高中化学 来源: 题型:
已知氧化性:Br2>Fe3+>I2;还原性:I﹣>Fe2+>Br﹣,则下列反应能发生的是( )
|
| A. | I2+2Fe2+═2Fe3++2I﹣ | B. | 2Br﹣+I2═Br2+2I﹣ |
|
| C. | 2Fe3++2I﹣═2Fe2++I2 | D. | 2Fe3++2Br﹣═2Fe2++Br2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
碱性电池具有容量大、放电电流大的特点,因而得到广泛应用。锌—锰碱性电池以氢氧化钾溶液为电解液,电池总反应式为: Zn(s)+2MnO2(s)+H2O(l) Zn(OH)2(s)+Mn2O3(s) 下列说法错误的是
A 电池工作时,锌失去电子
B 电池正极的电极反应式为:2MnO2(s)+H2O(1)+2e—=Mn2O3(s)+2OH—(aq)
C 电池工作时,电子由正极通过外电路流向负极
D 外电路中每通过0.2mol电子,锌的质量理论上减小6.5g
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com