
| ѡ�� | ʵ����ʵ | ���� |
| A | Na2S2O3��Һ��ϡH2SO4��Һ���ʱ������������ͬ��Na2S2O3��ҺŨ��Խ���������������ʱ��Խ�� | ��������������ʱ������Ӧ��Ũ�Ȼ�ѧ��Ӧ���ʼӿ� |
| B | �ڻ�ѧ��Ӧǰ�����������ͻ�ѧ���ʶ�û�з����ı� | ����һ�����μӻ�ѧ��Ӧ |
| C | ��NH4Cl������Ba(OH)2.8H2O�����Ϻ���ĥ���ձ����¶Ƚ��� | �÷�ӦΪ���ȷ�Ӧ |
| D | ���ݻ��ɱ���ܱ������з�����Ӧ H2��g��+ I2��g��  2HI��g���� 2HI��g�������ݻ���Сһ�� | ����Ӧ���ʼӿ죬�淴Ӧ���ʲ��� |
 ��1����Ԫ�¿�������ĩϵ�д�
��1����Ԫ�¿�������ĩϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��


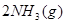 ��H=
��H=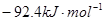 �����¡��������ݻ���ͬ�������ܱ�����A��B��A��ͨ��1molN2��3 molH 2��B ��ͨ��0.5 molN2��1.5 mol H 2����Ӧһ��ʱ���A��B�о��ﵽƽ��״̬�������ж���ȷ���ǣ� ��
�����¡��������ݻ���ͬ�������ܱ�����A��B��A��ͨ��1molN2��3 molH 2��B ��ͨ��0.5 molN2��1.5 mol H 2����Ӧһ��ʱ���A��B�о��ﵽƽ��״̬�������ж���ȷ���ǣ� ��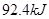

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A������������һ�����ڷ�Ӧ�������� |
| B����ͬ�����£�2mol��ԭ�������е�����С��1mol����������е����� |
| C�����ݸ�˹���ɣ��ɼ���ijЩ����ֱ�Ӳⶨ�Ļ�ѧ��Ӧ�ķ�Ӧ�ʱ� |
D��ͬ��ͬѹ�£� �ڹ��պ͵�ȼ������ �ڹ��պ͵�ȼ������ ��ͬ ��ͬ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
 2CO(g) ��H��0 ����Ӧ����Ϊ u1��N2��3H2
2CO(g) ��H��0 ����Ӧ����Ϊ u1��N2��3H2 2NH3 ��H��0��Ӧ����Ϊ u2������������Ӧ�����¶�����ʱ��u1��u2�ı仯���Ϊ �� ��
2NH3 ��H��0��Ӧ����Ϊ u2������������Ӧ�����¶�����ʱ��u1��u2�ı仯���Ϊ �� �� | A��ͬʱ���� | B��ͬʱ��С | C������С | D����С������ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A������ͬ�������£����ױȰ����ȶ� |
| B������ͬ�������£����ױȺ����ȶ� |
| C�����Ͱ��Ľṹ��ͬ |
| D��������������ȼ����������ȼ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ������
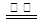 CO2(g)����H��E1 ��
CO2(g)����H��E1 ��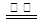 H2O(g)����H��E3 ��
H2O(g)����H��E3 ��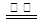 CO2(g)����H��E4�ܡ����Իش��������⣺
CO2(g)����H��E4�ܡ����Իش��������⣺ _____������ڡ��������ڡ�����С�ڡ���;��II�ų���������
_____������ڡ��������ڡ�����С�ڡ���;��II�ų��������� ��_____________________________________��
��_____________________________________���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ������

 OH)3��+�� ��H2Te��
OH)3��+�� ��H2Te���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ������
| �¶�/�� | 200 | 300 | 400 | 500 | 600 |
| ������/% | 89.9 | 71.0 | 47.0 | 26.4 | 13. 8 8 |
 2NH3��2 min�ﵽƽ��״̬ʱ��H2ת������50%�����¶��µ�ƽ�ⳣ��K��______________(�÷�����ʾ)����ʹK�����Բ�ȡ�Ĵ�ʩ��___________________��
2NH3��2 min�ﵽƽ��״̬ʱ��H2ת������50%�����¶��µ�ƽ�ⳣ��K��______________(�÷�����ʾ)����ʹK�����Բ�ȡ�Ĵ�ʩ��___________________��
 2NH3(l) ��H=___________��
2NH3(l) ��H=___________���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
 S>0����
S>0����| A��CaCO3(S)�ֽ�ΪCaO(S)��CO2(g) | B��2C2H6(g)��7O2(g)===4CO2(g)��6H2O(g) |
| C��NH4NO3(s)===NH(aq)��NO(aq) | D��Cl2===2Cl |
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com