下列说法正确的是( )
A.NaCl是电解质,所以NaCl可以导电
B.CO2能溶于水,且水溶液能导电,所以CO2是电解质
C.BaSO4难溶于水,故将BaSO4放入水中存在电离平衡
D.NaHCO3仅能在水溶液中导电
【答案】
分析:电解质是在水溶液里或熔融状态下能导电的化合物,且能导电的离子是其本身电离的;导电能力大小与离子浓度、离子所带电荷有关,浓度越大电荷越大,导电能力越强.
解答:解:电解质是在水溶液里或熔融状态下能导电的化合物,且能导电的离子是其本身电离的;导电能力大小与离子浓度、离子所带电荷有关,浓度越大电荷越大,导电能力越强.
A、虽然氯化钠是电解质,但必须形成自由移动的离子才能导电,故A错误.
B、二氧化碳的水溶液能导电,是因为二氧化碳溶于水,与水反应生成H
2CO
3,H
2CO
3电离出H
+、HCO
3-等使溶液导电,自由移动的离子并不是二氧化碳自身电离的离子,碳酸是电解质,CO
2是共价化合物,其液态没有自由移动的离子,CO
2是非电解质,故B错误.
C、虽然硫酸钡难溶于水,但硫酸钡是强电解质,强弱电解质与溶解度大小和溶液导电能力大小无关,只与电离程度有关,完全电离是强电解质,部分电离是弱电解质,溶解的硫酸钡在溶液中完全电离,不存在平衡.故C错
D:NaHCO
3是盐,属于强电解质,能在水溶液中导电,碳酸氢钠加热到一定温度就分解了,2NaHCO
3 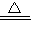
Na
2CO
3+CO
2↑+H
2O得到碳酸钠,二氧化碳和水,没有熔融态.故D对
故选D
点评:本题考查的是电解质的定义、影响导电能力大小的因素,但必须明确:导电能力强的溶液不一定是强电解质溶液,强电解质溶液的导电能力不一定强.

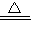 Na2CO3+CO2↑+H2O得到碳酸钠,二氧化碳和水,没有熔融态.故D对
Na2CO3+CO2↑+H2O得到碳酸钠,二氧化碳和水,没有熔融态.故D对

 课时掌控随堂练习系列答案
课时掌控随堂练习系列答案 一课一练一本通系列答案
一课一练一本通系列答案 浙江之星学业水平测试系列答案
浙江之星学业水平测试系列答案
 Sn(s,白)△H3=+2.1kJ?mol-1,
Sn(s,白)△H3=+2.1kJ?mol-1,