
����Ŀ���л���A(C5H10O2)���й���ζ,������ʳƷ�����,����������Ȼ�ͺϳ���֬���ܼ���
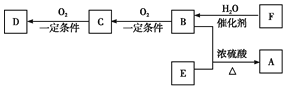
��֪:��B��E������û��֧��;��D����̼��������Һ��Ӧ�ų�������̼;��D��E������ͬ������;E����Է���������D��14;��F����ʹ������Ȼ�̼��Һ��ɫ��
(1).B�Ļ�ѧ����Ϊ__________��D�����������Ĺ����ŵ�������__________��
(2).B��E����A�ķ�Ӧ������__________��
(3).д��Fʹ������Ȼ�̼��Һ��ɫ�Ļ�ѧ��Ӧ����ʽ:__________��
(4).A�Ľṹ��ʽΪ__________��
(5).д��B��Na��Ӧ�Ļ�ѧ����ʽ:__________��
���𰸡��Ҵ� �Ȼ� ������Ӧ(��ȡ����Ӧ) CH2=CH2+Br2![]() CH2BrCH2Br CH3CH2COOCH2CH3 2CH3CH2OH+2Na
CH2BrCH2Br CH3CH2COOCH2CH3 2CH3CH2OH+2Na![]() 2CH3CH2ONa+H2��
2CH3CH2ONa+H2��
��������
�л���A(C5H10O2)���й���ζ����A�к��еĹ�����Ϊ������������ϳɷ��������Կ�����D����̼��������Һ��Ӧ�ų�������̼����֪DΪ�ᣬCΪȩ��BΪ����D��E��Ϊ������ͬ�����ŵ�ͬ���칹����E����Է���������D��14������A�ķ���ʽ��B��E������û��֧����֪��EΪ���ᣬDΪ���ᣬ��CΪ��ȩ��BΪ�Ҵ�����FΪ��ϩ��AΪCH3CH2COOCH2CH3���ݴ˷�������
��������������֪��
��1��B�Ļ�ѧ����Ϊ�Ҵ���DΪ���ᣬ������������Ĺ����ŵ��������Ȼ���
��2��.B��E����A�Ĺ���Ϊ���봼����������Ӧ��������ˮ�Ĺ��̣����䷴Ӧ����Ϊ��������Ӧ(��ȡ����Ӧ)��
��3��F�к�̼̼˫�������巢���ӳɷ�Ӧ���仯ѧ����ʽΪ��CH2=CH2+Br2![]() CH2BrCH2Br��
CH2BrCH2Br��
��4��A�Ľṹ��ʽΪ��CH3CH2COOCH2CH3��
��5���Ҵ����Ʒ�Ӧ�����Ҵ������������仯ѧ����ʽΪ��2CH3CH2OH+2Na![]() 2CH3CH2ONa+H2����
2CH3CH2ONa+H2����


 ȫ�ܲ����ĩС״Ԫϵ�д�
ȫ�ܲ����ĩС״Ԫϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����淴ӦH2��g����I2��g��![]() 2HI��g���ﵽƽ��ı�־�ǣ� ��
2HI��g���ﵽƽ��ı�־�ǣ� ��
A. v��H2��:v��HI��=1:2
B. H2��I2��HI���Ӹ�����Ϊ1:1:2
C. ���������I2��H2������������
D. ����������ɫ���ٸı�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���ش���������
��I���������и������ʣ�
��O2��O3 ��CH2=CH��CH3��CH2=CH��CH=CH2 ��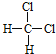 ��
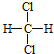
��
��![]() ��
��![]() ��CH3CH2CH3��CH3C��CH3��3
��CH3CH2CH3��CH3C��CH3��3
��![]() ��������Ϊ238������Ϊ146��ԭ�� ��CH3COOH��HCOOCH3
��������Ϊ238������Ϊ146��ԭ�� ��CH3COOH��HCOOCH3
��Ҫ����������
��1������ͬϵ�����________������ͬλ�ص���________������ͬ���칹�����________������ͬ�����������______������ͬ�����ʵ���________��
��II��������۲���ͼ��Ȼ��ش����⣮
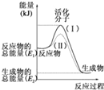
��2����ͼ����ʾ��Ӧ��______������ȡ����ȡ�����Ӧ��
��3����֪��1mol H��H����1mol I��I��1mol H��I���ֱ���Ҫ���յ�����Ϊ436kJ��151kJ��299kJ������1mol������1mol �ⷴӦ����HI��___����ų��������ա���___kJ��������
��4�����з�Ӧ�У��������ȷ�Ӧ����_____��
������ȼ�� ��ըҩ��ը ������кͷ�Ӧ �ܶ�����̼ͨ�����ȵ�̼
��ʳ�������������� ��Ba��OH��2��8H2O��NH4Cl��Ӧ ��������ϡ���ᷴӦ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����Ѵﵽƽ��ķ�Ӧ4NH3(g)��6NO(g)5N2(g)+6H2O( g) ��Сѹǿ��������Ӱ����
A.�����淴Ӧ���ʶ���С��ƽ��������Ӧ�����ƶ�
B.����Ӧ���ʼ�С���淴Ӧ��������ƽ�����淴Ӧ�����ƶ�
C.����Ӧ���������淴Ӧ���ʼ�С��ƽ��������Ӧ�����ƶ�
D.�����淴Ӧ���ʶ�����ƽ�ⲻ�����ƶ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������Ǽס��ҡ�����λͬѧ�Ʊ����������Ĺ���,������벢Э������������ʵ������
��ʵ��Ŀ�ģ� ��ȡ��������
(1).��ʵ��ԭ���� �ס��ҡ�����λͬѧ����ȡ�Ҵ���������Ũ�����Ϲ��ȵķ�����ȡ��������,Ũ��������ˮ����__________��
(2).��װ����ƣ��ס��ҡ�����λͬѧ�ֱ��������������ʵ��װ��:
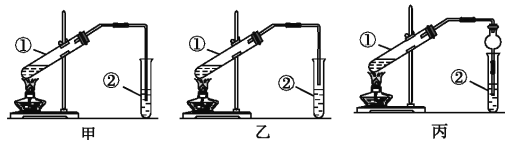
��Ӽס�����λͬѧ��Ƶ�װ����ѡ��һ����Ϊʵ������ȡ����������װ��,Ӧѡ���װ����______(����������������)����ͬѧ����װ���еIJ����ܸij������θ����,��������������,��һ��Ҫ������__________��
��ʵ�鲽�裩
�ٰ���ѡ���װ����װ����,���Թ����ȼ���3mL�Ҵ�,Ȼ������Թܢٱ���������2mLŨH2SO4��2mL����;
�ڽ��Թܢٹ̶���������;
�����Թܢ��м��������ı���Na2CO3��Һ;
���þƾ��ƶ��Թܢٻ�������;
�ݵ��۲쵽�Թܢ�������������ʱֹͣʵ�顣
(3).���������ۣ�
a.����(1)װ��ʵ��װ��,������Ʒǰ��Ӧ���__________;
b.�����Թܢ��й۲쵽������,��֪��������������������:��ɫ��״Һ�塢__________;
c.�Թܢ��з��������������ʵ�������__________��
d.д���Ʊ����������Ļ�ѧ����ʽ:__________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��X��Y��Z��W����ͼ��ʾ��ת����ϵ(��Ӧ�����Ͳ���������Ӧ��ʡ��)����X��Y��Z������

��Na��Na2O��Na2O2 ��AlCl3��Al(OH)3��NaAlO2 ��Fe��FeCl2��FeCl3 ��NaOH��Na2CO3��NaHCO3 ��C��CO��CO2
A. �ڢ� B. �٢ۢ� C. �٢ڢܢ� D. �٢ڢۢܢ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������Ϊ�����ṩ������Ӫ�������У����ڸ߷��ӻ��������
A. ���� B. ��֬ C. ������ D. ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ȼ�ϵ����һ�����͵Ļ�ѧ��Դ���乹����ͼһ��ʾ��a��b�����缫���ɶ��̼�Ƴɣ�ͨ��������ɿ�϶���ݳ������ڵ缫����ŵ硣
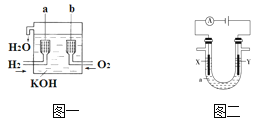
��1��a�缫��Ӧʽ��_______________________��
��2����ȼ�ϵ��������360 kg��ˮ�����·��ͨ����_____________mol�ĵ��ӡ�
��3������ͼ����ʾ��ⷽ��������ͭ�����Һaѡ��CuSO4��Һ����
��X�缫��Ӧʽ��___________________��
��Y�缫�IJ�����______________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����ᶡ������Ҫ�Ļ���ԭ�ϣ�����ˮ����ζ��ʵ�����Ʊ����ᶡ��(CH3COOCH2CH2CH2CH3)�ķ�Ӧװ��ʾ��ͼ���й���Ϣ���£�
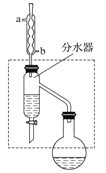
���� | ������ | ���ᶡ�� | |
�۵�/�� | 16.6 | ��89.5 | ��73.5 |
�е�/�� | 117.9 | 117 | 126.0 |
�ܶ�/g��cm��3 | 1.1 | 0.80 | 0.88 |
(1)���ᶡ���ֲ�Ʒ���Ʊ�
�ڸ����50 mLԲ����ƿ�У�װ���ʯ������12.0 mL��������16.0 mL������(����)���ټ�3��4��Ũ���ᡣȻ���ٰ�װ��ˮ��(���ã�ʵ������в��Ϸ����ȥ��Ӧ���ɵ�ˮ)�������ܣ�Ȼ��С����ȡ�д���Ʊ����ᶡ���Ļ�ѧ����ʽ_________������ƿ�з�Ӧ��Ļ������ȴ���ˮ��������ϲ���װ������ˮӦ��________(�a����b��)��ͨ�룻ͨ����ˮ�����Ϸ����ȥ��Ӧ���ɵ�ˮ��Ŀ����_____________��(2)���ᶡ���ľ���
�����ᶡ���ֲ�Ʒ�����µIJ������о��ƣ���ˮϴ������������ˮMgSO4�������10%̼����ϴ�ӡ�����ȷ�IJ���������________________(����)��
A.�٢ڢۢ� B.�ۢ٢ܢ� C.�ܢ٢ۢ� D.�ۢܢ٢�
�������ᶡ���ľ����У���10%̼����ϴ�ӵ���ҪĿ����_________��
����ϴ�ӡ���Һ�����У�Ӧ�����Ȼ���ã����ֲ��________(����)��
a.ֱ�ӽ����ᶡ���ӷ�Һ©�����Ͽڵ���
b.ֱ�ӽ����ᶡ���ӷ�Һ©�����¿ڷų�
c.�Ƚ�ˮ��ӷ�Һ©�����¿ڷų����ٽ����ᶡ�����¿ڷų�
d.�Ƚ�ˮ��ӷ�Һ©�����¿ڷų����ٽ����ᶡ�����Ͽڵ���
(3)�������
������ˮ�����������붡����Ӧ���ɵ�ˮ���Ϊ1.8 mL����������ȡ���ᶡ�������з�Ӧ���������û����ʧ���Һ��Ը���Ӧ�����ᶡ���IJ���Ϊ________��
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com