
���� ��1���ٿ��淴Ӧ�ﵽƽ��״̬ʱ�����淴Ӧ������ȣ���Ӧ��ϵ�и����ʵ����ʵ��������ʵ���Ũ�ȡ��ٷֺ����Լ��ɴ������һϵ�����������䣻
�ڼ���NO��ƽ�������ƶ�����ת����NO���ʵ���ԶԶС�ڼ����NO��
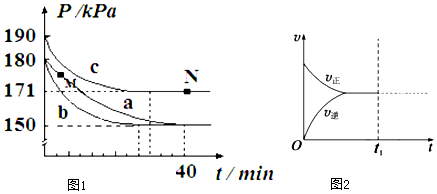
��2����ʵ��a�У�ͬ��ͬ���£���������ѹǿ֮�ȵ��������ʵ���֮�ȣ���ʼʱѹǿΪ180kPa��ƽ��ʱΪ150kPa�����Է�Ӧǰ����������ʵ���֮��=180kPa��150kPa=6��5����Ӧǰ����������ʵ���=��0.4+0.2��mol=0.6mol����Ӧ������������ʵ���Ϊ0.5mol������2NO2��g��+O3��g��?N2O5��g��+O2��g��֪����Ӧǰ����ٵ����ʵ������ڳ����μӷ�Ӧ�����ʵ���Ϊ��0.6-0.5��mol=0.1mol��
����v=$\frac{��c}{��t}$���������Ӧ���ʣ�
ʵ��c�У���Ӧǰѹǿ�뷴Ӧǰ��ѹǿ�仯��֮�ȵ��ڷ�Ӧǰ��������ʵ����뷴Ӧǰ����������ʵ����仯��֮��=190pKa����190-171��pKa=10��1����Ӧǰ����������ʵ���=��0.4+0.2��mol=0.6mol����ǰ��������ٵ����ʵ���Ϊ0.06mol���μӷ�Ӧ�Ķ����������ʵ����Ƿ�Ӧǰ����ٵ����ʵ�����2����Ϊ0.12mol��
��������ת����=$\frac{�μӷ�Ӧ�Ķ����������ʵ���}{����������ʼ���ʵ���}��100%$��
����ʵ��a��ȣ�b�����̵���ƽ���ʱ�䣬��ƽ��ʱѹǿ���䣬˵���ı�����ֻ�ı䷴Ӧ���ʵ���Ӱ��ƽ���ƶ���
c�иı�����ʱ����Ӧ�����ҷ�Ӧǰ��ѹǿ�ı�����С������ƽ�������ƶ���
���¶�Խ�ߡ�ѹǿԽ��Ӧ����Խ���¶ȶԻ�ѧ��Ӧ����Ӱ�����ѹǿ�Ի�ѧ��Ӧ����Ӱ�죻
������N��ʱ��ά���¶Ⱥ�ѹǿ���䣬t1ʱ�ټ���0.4molNO2��0.2mol O3���ı�����˲�䣬��Ӧ��Ũ�Ȳ��䡢������Ũ�ȱ�С��ƽ�������ƶ���
��� �⣺��1��C��s��+2NO��g��?N2��g��+CO2��g����H��0��
��A����������NO��=2������CO2��ʱ�÷�Ӧ�ﵽƽ��״̬������2������NO��=������CO2��ʱ�÷�Ӧû�дﵽƽ��״̬���ʴ���
B���÷�Ӧǰ���������ʵ������䣬�����ں��¡����ݵ������У���������ѹǿʼ�ձ��ֲ��䣬�����жϸ÷�Ӧ�Ƿ�ﵽƽ��״̬���ʴ���
C���ھ��ȡ����ݵ������У���Ӧ��ƽ�ⳣ�����ٱ仯��˵���÷�Ӧ���淴Ӧ������ȣ��÷�Ӧ�ﵽƽ��״̬������ȷ��
D���ں��¡���ѹ�������У���Ӧǰ����������������仯�������������ܶȱ��ֲ���ʱ���÷�Ӧ�ﵽƽ��״̬������ȷ��
��ѡCD��
�ڼ���NO��ƽ�������ƶ�����ת����NO���ʵ���ԶԶС�ڼ����NO�����»�������е������ӵ����ʵ���ԶԶС�������ʵ������ӵ��������Ե���������С���ʴ�Ϊ����С��
��2����ͬ��ͬ���£���������ѹǿ֮�ȵ��������ʵ���֮�ȣ���ʼʱѹǿΪ180kPa��ƽ��ʱΪ150kPa�����Է�Ӧǰ����������ʵ���֮��=180kPa��150kPa=6��5����Ӧǰ����������ʵ���=��0.4+0.2��mol=0.6mol����Ӧ������������ʵ���Ϊ0.5mol������2NO2��g��+O3��g��?N2O5��g��+O2��g��֪����Ӧǰ����ٵ����ʵ������ڳ����μӷ�Ӧ�����ʵ���Ϊ��0.6-0.5��mol=0.1mol��
����ƽ����Ӧ����v=$\frac{��c}{��t}$=$\frac{\frac{0.1mol}{10L}}{40min}$=2.5��10-4 mol•L-1•min-1��
ʵ��c�У���Ӧǰѹǿ�뷴Ӧǰ��ѹǿ�仯��֮�ȵ��ڷ�Ӧǰ��������ʵ����뷴Ӧǰ����������ʵ����仯��֮��=190pKa����190-171��pKa=10��1����Ӧǰ����������ʵ���=��0.4+0.2��mol=0.6mol����ǰ��������ٵ����ʵ���Ϊ0.06mol���μӷ�Ӧ�Ķ����������ʵ����Ƿ�Ӧǰ����ٵ����ʵ�����2����Ϊ0.12mol��
��������ת����=$\frac{�μӷ�Ӧ�Ķ����������ʵ���}{����������ʼ���ʵ���}��100%$=$\frac{0.12mol}{0.4mol}$��100%=30%��
�ʴ�Ϊ��2.5��10-4 mol•L-1•min-1��30%��
����ʵ��a��ȣ�b�����̵���ƽ���ʱ�䣬��ƽ��ʱѹǿ���䣬˵���ı�����ֻ�ı䷴Ӧ���ʵ���Ӱ��ƽ���ƶ������Ըı��������ʹ�ô�����
c�иı�����ʱ����Ӧ�����ҷ�Ӧǰ��ѹǿ�ı�����С������ƽ�������ƶ������Ըı�������������¶ȣ�
�ʴ�Ϊ��ʹ�ô����������¶ȣ�
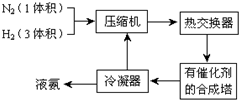
���¶�Խ�ߡ�ѹǿԽ��Ӧ����Խ���¶ȶԻ�ѧ��Ӧ����Ӱ�����ѹǿ�Ի�ѧ��Ӧ����Ӱ�죬N���¶ȸ���M�㣬����M����淴Ӧ���� v���棩��N�������Ӧ����v���������ʴ�Ϊ������
������N��ʱ��ά���¶Ⱥ�ѹǿ���䣬t1ʱ�ټ���0.4molNO2��0.2mol O3���ı�����˲�䣬��Ӧ��Ũ�Ȳ��䡢������Ũ�ȱ�С��ƽ�������ƶ�����ͼ��Ϊ ���ʴ�Ϊ��
���ʴ�Ϊ�� ��
��
���� ���⿼�黯ѧƽ����㼰��ѧƽ��Ӱ�����أ�Ϊ��Ƶ���㣬���ؿ���ѧ��ͼ�����������������ע�⣨2������C�����϶�������ת���ʵļ��㷽����ע�⣨2�����к��º�ѹ�����¼��뷴Ӧ��ᵼ������������ı����˲�䷴Ӧ��Ũ�Ȳ��䵫������Ũ�ȼ�С��Ϊ�״��㣮



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ����
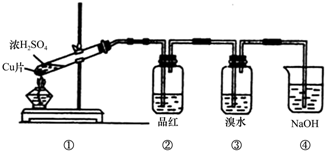
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ���ȷ�Ӧ�ڳ�����һ���Ǻ������� | |
| B�� | ��Ҫ���Ȳ��ܷ����ķ�Ӧһ�������ȷ�Ӧ | |
| C�� | ��C��ʯī����C�����ʯ����H=+1.9 kJ•mol-1��֪�����ʯ��ʯī�ȶ� | |
| D�� | �������������������ֱ���ȫȼ�գ�ǰ�߷ų��������� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 2022 kJ | B�� | 2670 kJ | C�� | 1698kJ | D�� | 2346 kJ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 16g�����ͳ����Ļ�����к��е���ԭ����ΪNA | |
| B�� | ��״���£�22.4 Lˮ�к��е���ԭ����ΪNA | |
| C�� | NA���������ӵ����Ϊ22.4L | |
| D�� | ���ʵ���Ũ��Ϊ0.5 mol/L��MgCl2��Һ�У����е�Cl-����ΪNA |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
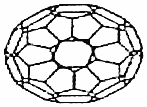
| A�� | C60��Ħ��������720 g•moL-1 | |
| B�� | 1 mol C60��ȫȼ������22.4 L CO2 | |
| C�� | C60����������� | |
| D�� | C60�Ľṹ����ʯһ�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��ˮ�����ᡢ�����ᱵ | B�� | ˮ�������ᡢ�ռ�������� | ||
| C�� | ͭ�����ᡢʯ��ʯ���Ȼ�ͭ | D�� | ���������ᡢ������� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com