
【题目】不能由单质直接与O2反应生成的氧化物是( )
A. Fe3O4B. NO2C. SO2D. CuO
科目:高中化学 来源: 题型:
【题目】在t℃时,某NaOH稀溶液中,c(H+)=10﹣a mol/L,c(OH﹣)=10﹣b mol/L,已知a+b=13,则在该温度下,将100mL 0.10mol/L的稀硫酸与100mL 0.40mol/L的NaOH溶液混合后,溶液的pH为(已知:忽略混合时体积的变化;lg2=0.30;lg3=0.48)( )
A.11.52
B.11.70
C.11.82
D.12.00
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在t℃时,某NaOH稀溶液中,c(H+)=10﹣a mol/L,c(OH﹣)=10﹣b mol/L,已知a+b=13,则在该温度下,将100mL 0.10mol/L的稀硫酸与100mL 0.40mol/L的NaOH溶液混合后,溶液的pH为(已知:忽略混合时体积的变化;lg2=0.30;lg3=0.48)( )
A.11.52
B.11.70
C.11.82
D.12.00
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某同学用50mL 0.50mol/L的盐酸与50mL 0.55mol/L的NaOH溶液在有图所示的装置中进行中和反应,通过测定反应过程中所放出的热量计算中和热.下列说法正确的是( ) 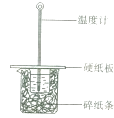
A.实验过程中没有热量损失
B.烧杯间填满碎纸条的作用是固定小烧杯
C.图中实验装置缺少环形玻璃搅拌棒
D.若将盐酸体积改为60mL,理论上所求中和热不相等
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某同学利用如图所示的实验装置进行铁跟水蒸气反应的实验,并继续研究铁及其化合物的部分性质. 请回答下列问题:
(1)装置中湿棉花的作用 . 硬质试管中发生反应的化学方程式为 .
(2)该同学欲确定反应后硬质试管中固体物质的成分,设计了如下实验方案: ①待硬质试管冷却后,取少许其中的固体物质溶于稀硫酸得溶液B;
②取少量溶液B滴加KSCN溶液,若溶液变红色则说明硬质试管中固体物质的成分是 .
若溶液未变红色,则说明硬质试管中固体物质的成分是 .
(3)该同学按上述实验方案进行了实验,结果溶液未变红色,原因是: . (用离子方程式表示).
(4)该同学马上另取少量溶液B,使其跟NaOH溶液反应.若按如图所示的操作,可观察到生成白色沉淀,迅速变成灰绿色,最后变成红褐色的现象,请写出白色沉淀变成红褐色沉淀所发生发应的化学方程式: .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知水在25℃和95℃时,其电离平衡曲线如图所示: 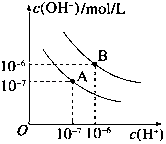
(1)95℃时水的离子积KW=
(2)95℃时,0.01mol/LNaOH溶液的PH= .
(3)95℃时水的电离平衡曲线应为(填“A”或“B”),请说明理由 .
(4)25℃时,将pH=9的NaOH溶液与pH=4的H2SO4溶液混合,若所得混合溶液的pH=7,则NaOH溶液与H2SO4溶液的体积比为 .
(5)95℃时,若100体积pH1=a的某强酸溶液与1体积pH2=b的某强碱溶液混合后溶液呈中性,则混合前,该强酸的pH1与强碱的pH2之间应满足的关系是 .
(6)曲线B对应温度下,pH=2的某HA溶液和pH=10的NaOH溶液等体积混合后,混合溶液的pH=5.请分析原因: .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知水在25℃和95℃时,其电离平衡曲线如图所示: 
(1)95℃时水的离子积KW=
(2)95℃时,0.01mol/LNaOH溶液的PH= .
(3)95℃时水的电离平衡曲线应为(填“A”或“B”),请说明理由 .
(4)25℃时,将pH=9的NaOH溶液与pH=4的H2SO4溶液混合,若所得混合溶液的pH=7,则NaOH溶液与H2SO4溶液的体积比为 .
(5)95℃时,若100体积pH1=a的某强酸溶液与1体积pH2=b的某强碱溶液混合后溶液呈中性,则混合前,该强酸的pH1与强碱的pH2之间应满足的关系是 .
(6)曲线B对应温度下,pH=2的某HA溶液和pH=10的NaOH溶液等体积混合后,混合溶液的pH=5.请分析原因: .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有机物相关描述不正确的( )
A.按照有机物系统命名法,化合物 ![]() 的名称为:3,3﹣二乙基戊烷
的名称为:3,3﹣二乙基戊烷
B.甲醇、乙二醇、丙三醇都为饱和醇,熔沸点依次递增
C.甘氨酸H2N﹣CH2COOH、丙氨酸CH3CH(NH2)COOH、谷氨酸HOOCCH2CH2CH(NH2)COOH一定条件下形成链状三肽的结构最多有33种
D.分子式为C5H10O2的所有酯类的同分异构体共有9种
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】NH3在工业生产上有重要的应用
(1)写出用浓氨水检验氯气管道泄漏的化学反应方程式
(2)若将少量氨气与过量氯气混合,则生成一种酸和另一种化合物A,A中所有原子均满足8电子稳定结构,试写出A的电子式;A在一定条件下能与水反应,可用于饮用水的消毒,试写出此反应的化学反应方程式 .
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com