

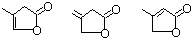





 和
和 ,由题意可知B为
,由题意可知B为 ,D为
,D为 ,则C为苯酚,E为
,则C为苯酚,E为 ,在浓硫酸作用下发生消去反应和酯化反应,F可能为
,在浓硫酸作用下发生消去反应和酯化反应,F可能为 ,结合有机物的结构和性质解答该题.
,结合有机物的结构和性质解答该题. 和
和 ,由题意可知B为
,由题意可知B为 ,D为
,D为 ,则C为苯酚,E为
,则C为苯酚,E为 ,在浓硫酸作用下发生消去反应和酯化反应,F可能为
,在浓硫酸作用下发生消去反应和酯化反应,F可能为 ,
, ,在浓硫酸作用下发生消去反应可生成三种位置不同的C=C,并能发生酯化反应,F可能为
,在浓硫酸作用下发生消去反应可生成三种位置不同的C=C,并能发生酯化反应,F可能为 ,
, ;
; 和
和 ,反应的方程式为
,反应的方程式为 ,
, ;
; ,含有-OH和-COOH,并且含有两种不同位置的-OH,发生缩聚反应产物可能有
,含有-OH和-COOH,并且含有两种不同位置的-OH,发生缩聚反应产物可能有 ,
, .
.

 名师指导期末冲刺卷系列答案
名师指导期末冲刺卷系列答案科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com