
CO2��CH4��������Ҫ���������壬ͨ��CH4��CO2��Ӧ�������ֵ��ѧƷ��Ŀǰ���о�Ŀ�ꡣ
��1��250��ʱ�������Ͻ�Ϊ��������4 L������ͨ��6 mol CO2��6 mol CH4���������·�Ӧ��CO2 (g)��CH4(g) 2CO(g)��2H2(g)��ƽ����ϵ�и��������������±���
2CO(g)��2H2(g)��ƽ����ϵ�и��������������±���
| ���� | CH4 | CO2 | CO | H2 |
| ������� | 0.1 | 0.1 | 0.4 | 0.4 |
�ٴ��¶��¸÷�Ӧ��ƽ�ⳣ��K=__________
����֪��CH4(g)��2O2(g)��CO2(g)��2H2O(g) ��H=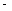 890.3 kJ·mol��1
890.3 kJ·mol��1
CO(g)��H2O (g)��CO2(g)��H2 (g) ��H=+2.8 kJ·mol��1
2CO(g)��O2(g)��2CO2(g) ��H=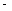 566.0 kJ·mol��1
566.0 kJ·mol��1
��ӦCO2(g)��CH4(g) 2CO(g)��2H2(g) �ġ�H=________________
2CO(g)��2H2(g) �ġ�H=________________
��2���Զ������ѱ��渲��Cu2Al2O4Ϊ���������Խ�CO2��CH4ֱ��ת�������ᡣ
���ڲ�ͬ�¶��´����Ĵ�Ч���������������������ͼ��ʾ��250��300��ʱ���¶����߶�������������ʽ��͵�ԭ����_____________________
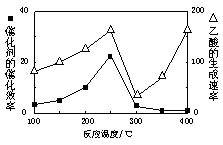
��Ϊ����߸÷�Ӧ��CH4��ת���ʣ����Բ�ȡ�Ĵ�ʩ��________________________
�۽�Cu2Al2O4�ܽ���ϡ�����е����ӷ���ʽΪ___________________________
��3��Li2O��Na2O��MgO��������CO2�������Ѱ������CO2���������ʣ����н����������______
a.���ڼ�����������Ѱ��
b.���ڢ�A����A��Ԫ���γɵ���������Ѱ��
c.���ھ���ǿ�����Ե�������Ѱ��
��Li2O����CO2�������ںϳ�Li4SiO4��Li4SiO4�������ա��ͷ�CO2��ԭ���ǣ���500�棬CO2��Li4SiO4�Ӵ�������Li2CO3��ƽ��������700�棬��Ӧ������У��ų�CO2��Li4SiO4������˵����ԭ���Ļ�ѧ����ʽ��___________________________
��4�����÷�ӦA�ɽ��ͷŵ�CO2ת��Ϊ���й�ҵ���ü�ֵ�IJ�Ʒ��
��ӦA��
���µ�⼼���ܸ�Чʵ�֣�3���з�ӦA������ԭ��ʾ��ͼ���£�
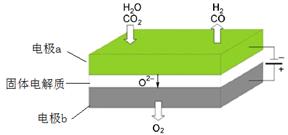
CO2�ڵ缫a�ŵ�ķ�Ӧʽ��_____________________________________________
��֪ʶ�㡿��Ӧ�ȵļ��㡢��ѧƽ�ⳣ���ĺ��塢��ѧƽ���Ӱ�����ء����ԭ��
���𰸽������Ţ�64 ��+247.3 kJ·mol��1
�Ƣ��¶ȳ���250��ʱ�������Ĵ�Ч�ʽ���
������Ӧѹǿ������CO2��Ũ��
��3Cu2Al2O4+32H++2NO3��=6Cu2++ 6Al3++2NO��+16 H2O
��3����ab ��1�֣� ��CO2 + Li4SiO4  Li2CO3 + Li2SiO3
Li2CO3 + Li2SiO3
��4��CO2 + 2e- == CO+O2-
��������1���� CO2��g��+CH4��g��⇌2CO��g��+2H2��g��
��ʼ��mol�� 6 6 0 0
��Ӧ��mol�� X X 2X 2X
ƽ�⣨mol�� 6-X 6-X 2X 2X
��CH4���������Ϊ0.1����(6-x)/(12+2x)=0.1�����X=4������K=(22��22)/(0.5��0.5)=64
��CH4��g��+2O2��g��=CO2��g��+2H2O��g����H=-890.3kJ•mol-1 ��
CO��g��+H2O ��g��=CO2��g��+H2 ��g����H=2.8kJ•mol-1 ��
2CO��g��+O2��g��=2CO2��g����H=-566.0kJ•mol-1 ��
���ݸ�˹���ɣ��ɢ�+�ڡ�2-�ۡ�2��
CO2��g��+CH4��g��⇌2CO��g��+2H2��g����H=(-890.3+2.8��2+566.0��2) kJ•mol-1=+247.3 kJ•mol-1��
��2�����¶ȳ���250��ʱ�������Ĵ�Ч�ʽ��ͣ������¶����߶�������������ʽ��ͣ�
������Ӧѹǿ������CO2��Ũ�ȣ�ƽ�������ƶ�����Ӧ��ת��������
��Cu2Al2O4������������ʽ��Cu2O•Al2O3�����ᷴӦ�������ӷ���ʽ��
3Cu2Al2O4+32H++2NO3-=6Cu2++6Al3++2NO��+16H2O��
��3����a��Li2O��Na2O��MgO�����ڼ��������������������������CO2�����ڼ�����������Ѱ������CO2���������ʣ���a��ȷ��
b��Li2O��Na2O��MgO��������CO2���ơ�þ����Ϊ��A����A��Ԫ�أ����Կ��ڢ�A����A��Ԫ���γɵ���������Ѱ������CO2���������ʣ���b��ȷ��
c��Li2O��Na2O��MgO��������CO2�������Ƕ�û��ǿ�����ԣ������ն�����̼��������ԭ�أ���c���� �ʴ�Ϊ��ab��
����500�棬CO2��Li4SiO4�Ӵ�������Li2CO3����Ӧ��ΪCO2��Li4SiO4����������Li2CO3�����������غ��֪���ﻹ��Li2SiO3�����Ի�ѧ����ʽΪCO2 + Li4SiO4  Li2CO3 + Li2SiO3��
Li2CO3 + Li2SiO3��
��4��������̼��a���õ����ӷ�����ԭ��Ӧ����һ����̼ͬʱ���������ӣ���Ӧ�缫��ӦʽΪ��CO2+2e-═CO+O2-��
��˼·�㲦��������Ҫ�������ۺ�����CO2���漰�Ȼ�ѧ��Ӧ���绯ѧ����ѧƽ��Ӱ�����صȣ���Ϊ�ۺϣ���Ŀ�Ѷ��е�


 �㾦�½̲�ȫ�ܽ��ϵ�д�
�㾦�½̲�ȫ�ܽ��ϵ�д� Сѧ�̲���ȫ���ϵ�д�
Сѧ�̲���ȫ���ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�������ӷ���ʽ��д��ȷ���� (����)
A����100 mLŨ��Ϊ1 mol·L��1�� Fe(NO3)3����Һ��ͨ������SO2
2Fe3����SO2��2H2O=2Fe2����SO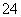 ��4H��
��4H��
B����100 mLŨ��Ϊ2 mol·L��1��FeI2����Һ��ͨ���״����5.6 L��Cl2
4Fe2����6I����5Cl2=4Fe3����3I2��10Cl��
C����NaHCO3��Һ�м�������ij���ʯ��ˮ
2HCO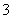 ��Ca2����2OH��=CaC
��Ca2����2OH��=CaC O3����2H2O��CO
O3����2H2O��CO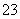
D����������Һ�м������������������Һ
Al3����2SO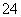 ��2Ba2����4OH��=2BaSO4����AlO
��2Ba2����4OH��=2BaSO4����AlO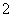 ��2H2O
��2H2O
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
��nAΪ�����ӵ���������ֵ������˵����ȷ����(����)
A����״���£�11.2 L��H2O�к���1.5nA��ԭ��
B��0.1 mol·L��1 ��(NH4)2SO4��Һ�У�����NH4����С��0.2nA
C�����³�ѹ�£�16 g��O2��O3��������У�����8nA������
D��������ͬ��N2��CO�У�����2nA��ԭ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
д�����и����ķ���ʽ��
(1)����B�ķ����к���200����ԭ��________��
(2)1 L����D��������ȫȼ��ʱ������ͬ��ͬѹ��15 L��ˮ����________��
(3)��֪�ڱ�״���£�ij��̬�����ܶ�Ϊ1.34 g��L��1����0.1 mol����̬�л�����ȼ������8.8 g CO2��5.4 g H2O________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
���û�ѧ��Ӧԭ��֪ʶ�ش������й�̼��̼�Ļ���������⣺
(1)����β������Ҫ��Ⱦ����NO�Լ�ȼ��ȼ�ղ���ȫ��������CO���������ִ������е���Ҫ������Ⱦ�Ϊ�˼�������β����ɵĴ�����Ⱦ�����ǿ�ʼ̽������NO��CO��һ��������ת��Ϊ����������E��F�ķ���(��֪�÷�Ӧ��H<0). ��2 L�ܱ������м���һ����NO��CO�����¶ȷֱ���T1��T2ʱ����ø�����ƽ��ʱ���ʵ������±���
T/�� n/mol | NO | CO | E | F |
��ʼ | 0.100 | 0.100 | 0 | 0 |
T1 | 0.020 | 0.020 | 0.080 | 0.040 |
T2 | 0.010 | 0.010 | 0.090 | 0.045 |
�������ϱ����ݣ�д��NO��CO��Ӧ�Ļ�ѧ����ʽ .
��������ӦT1��ʱ��ƽ�ⳣ��ΪK1��T2��ʱ��ƽ�ⳣ��ΪK2�����ݱ������ݼ���K1= �����ݱ��������жϣ��¶�T1��T2�Ĺ�ϵ��(�����)__________��
A��T1>T2B��T1<T2 C��T1=T2 D�����Ƚ�
(2)��Ӧ���ɵ�����E�������������������գ�����0.4molE������200mL 3mol/L NaOH��Һ������ȫ���գ���Һ������Ũ���ɴ�С��˳��Ϊ�� .
(3)��֪CH4��H2��CO��ȼ���ȷֱ�Ϊ890.3kJ/mol��285.8 kJ/mol��283.0 kJ/mol����ҵ��������Ȼ��(��Ҫ�ɷ���CH4)��CO2���и��������Ʊ�CO��H2��д���÷�Ӧ���Ȼ�ѧ����ʽ�� .
(4)CO����������ȼ�ϵ�ص�ȼ�ϣ�ij������ȼ�ϵ�ؾ��иߵķ���Ч�ʣ�����ܵ����ӣ��õ���� Li2CO3 �� Na2CO3 �������λ����������ʣ�COΪ����ȼ����������CO2 �Ļ����Ϊ������ȼ�����Ƶ��� 650 ���¹�����ȼ�ϵ�أ�д���为���������缫��Ӧ����ʽ�������� �������� .
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
п�̸ɵ�������������ʹ�������϶̣���Ϊһ���Ե�أ�����֮���������ӵ����ⲻ���˷��˱���Ľ�����Դ�����һ���������صĻ�����Ⱦ���±��Ǹ����ص��ۺϳɷַ��������
| Ԫ�� | п[��Դ��ȫ,Ʒ����&��*��+��] | �� | �� | ͭ | ̼ | ���� |
| �����ٷֺ��� | 13��27 | 14��28 | 23��26 | 0.5��0.7 | 5��6 | 13 |
ͨ���Ļ�е������������и���ֽ���������ȵķ��룬�Ӷ�ʹ�����������̵õ����ٷֱ��пƤ���̷ۣ�MnO2������ʪ��������ͨ��Ԥ��������ȡ�������ȹ����Ƴ���Ʒ��������������ͼ��
��������֪�����ӳ�����ȫ��pHΪ
| ���� | Fe3+ | Fe2+ | Cu2+ | Mn2+ |
| pH | 3.2 | 9.0 | 6.7 | 10.1 |
��֪��пԪ������Ԫ�����ƣ��������ԡ�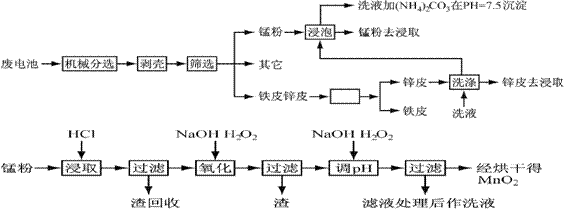
1������п�̸ɵ��Ϊ���Ե�أ��������ҺΪKOH,����������ӦΪ ��
�缫�ܷ�Ӧ����Ϊ ��
2����Ԥ�����У�������Ƥ��пƤ�ķ����� ��ϴҺ��(NH4)2CO3��pH��7.5������һ�ּ�ʽ�Σ������ʵĻ�ѧʽΪ ��
3���������������У�д������30%�����ܽ�ʱ�����ӷ���ʽ �������ܽ����յ����� ��
4����֪�ڶ��μ�H2O2�����pH��9��Ŀ��Ϊ��Mn2+ת��ΪMnO2,���һ�μ�H2O2�����pH��5��Ŀ���� ��
5��ʵ�������ø��������Һ����Mn2+ʱ��������ɫ�������÷�Ӧ�����ӷ���ʽΪ
��
6���������ڸ��������¿��Եõ�������������ȷֽ�ķ���ʽΪ ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�����Դ�뻷�������⣬
ȫ�������չ����Դ��ͬʱ�����������ܼ��š���̼���á���ش��������⣺
��������һ�������Դ����������ȡ�봢��������Դ����������о��ȵ㡣
��֪��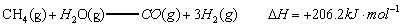
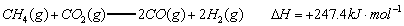
��1���Լ���Ϊԭ����ȡ�����ǹ�ҵ�ϳ��õ����ⷽ����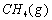 ��
��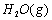 ��Ӧ����CO2(g)��
��Ӧ����CO2(g)��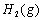 ���Ȼ�ѧ����ʽΪ ��
���Ȼ�ѧ����ʽΪ ��
��2���������CO(NH2)2�ļ�����Һ�����װ����ͼ��ʾ(�����и�Ĥ����ֹ����ͨ��������������Ϊ���Ե缫)�����ʱ�������ĵ缫��ӦʽΪ ��
��3��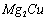 ��һ�ִ���Ͻ�350��ʱ��
��һ�ִ���Ͻ�350��ʱ��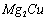 ��
��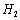 ��������
��������
Ӧ������MgCu2�ͽ���һ�ֽ���Ԫ�ص��⻯�����
�����������Ϊ0.077������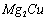 ��
��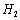 ��Ӧ�Ļ�ѧ
��Ӧ�Ļ�ѧ
����ʽΪ ������ ��
���ٵƾ���ʹ�������������ܻ������ŵ㡣һ���¶��£��ڵ��ٵƵ����ڷ���������������ڵ��ݱ��ϵ��ٿ��Է������淴Ӧ��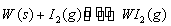 ��Ϊģ��÷�Ӧ����ʵ������ȷ��ȡ0.508 g�⡢0.6992 g�����ٷ�����50.0 mL�ܱ������У���һ���¶��·�Ӧ����ͼ�ǻ�������е�
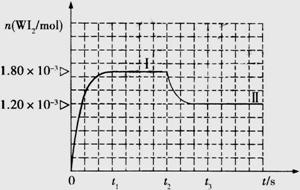
��Ϊģ��÷�Ӧ����ʵ������ȷ��ȡ0.508 g�⡢0.6992 g�����ٷ�����50.0 mL�ܱ������У���һ���¶��·�Ӧ����ͼ�ǻ�������е�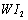 ���������ʵ�����ʱ��仯��ϵ��ͼ��
���������ʵ�����ʱ��仯��ϵ��ͼ�� ����������I(0��t2ʱ���)�ķ�Ӧ�¶�Ϊ450 �棬���ߢ�(��t2ʱ�̿�ʼ)�ķ�Ӧ�¶�Ϊ530�档
����������I(0��t2ʱ���)�ķ�Ӧ�¶�Ϊ450 �棬���ߢ�(��t2ʱ�̿�ʼ)�ķ�Ӧ�¶�Ϊ530�档
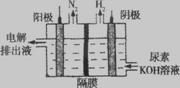
��4���÷�Ӧ�� ����д�����ȡ������ȡ�����Ӧ����450��ʱ���÷�Ӧ��ƽ
�ⳣ��K= �� ��
��5��������450���¶Ȳ��䣬����������ټ���0.508 g�⣬���ٴδﵽƽ��ʱ����Ӧ���������I2�İٷֺ��� �����������䡱��С������
��6��������450���¶Ȳ��䣬����������ټ���0.002 mol W��0.000 6 mol I2��0.0054 mol WI2����ѧƽ�� ��������ƶ����������ƶ����������ƶ�������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
���й�������Ӧ�õ�˵���������
A�����������ɳ���ʢ�Ÿ����� B�������������ϴ����
C��Ũ��ˮ�ɼ��������ܵ�©�� D��Na2S�ɳ�ȥ��ˮ�е�Cu2+
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com