
(1)将下列离子Na+、K+、Cu2+、H+、NO3﹣、Cl﹣、CO32﹣、OH﹣,按可能大量共存于同一溶液的情况,则分成A、B两组,而且每组中均含两种阳离子和两种阴离子,则A组 ,B组 .
用同浓度的AgNO3溶液分别与同浓度等体积的NaCl、MgCl2、AlCl3溶液反应,所用AgNO3溶液的体积比为 ;如用同浓度等体积的AgNO3溶液分别与等浓度的NaCl、MgCl2、AlCl3溶液反应,所用三种溶液的体积比为 .
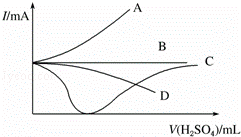
(3)向一定量的Ba(OH)2溶液中逐滴加入稀硫酸,直至过量,整个过程中混合溶液的导电能力(用电流强度I表示)近似的用下图中的曲线 表示.
考点: 离子共存问题;化学方程式的有关计算;电解质在水溶液中的电离.
分析: (1)A组和B组没有明确的要求,只要从离子能否大量共存的角度将离子分成两组即可;
均发生反应Ag++Cl﹣=AgCl↓,同浓度等体积的NaCl、MgCl2、AlCl3溶液反应,氯离子的物质的量比为1:2:3,所用AgNO3的物质的量比为1:2:3;若AgNO3的物质的量相等,MgCl2、KC1、A1Cl3三种溶液中Cl﹣的物质的量相等;
(3)溶液的导电能力取决于溶液中离子浓度的大小,根据氢氧化钡和硫酸的反应来确定离子浓度变化,进而确定导电能力的变化.
解答: 解:(1)设A组中含有Cu2+,Cu2+与CO32﹣、OH﹣分别反应生成沉淀而不能共存,CO32﹣、OH﹣则应存在于B组中,CO32﹣、OH﹣与H+反应而不能共存,则H+应存在于A组,
又每组中均含两种阳离子和两种阴离子,
所以A组中应还含有NO3﹣、Cl﹣,B组中还应含有Na+、K+,
所以A组中含有Cu2+、H+、Cl﹣、NO3﹣,B组中含有Na+、K+、OH﹣、CO32﹣ ( A、B可对换).
故答案为:Cu2+、H+、Cl﹣、NO3﹣;Na+、K+、OH﹣、CO32﹣ ( A、B可对换);
均发生反应Ag++Cl﹣=AgCl↓,同浓度等体积的NaCl、MgCl2、AlCl3溶液反应,氯离子的物质的量比为1:2:3,所用AgNO3的物质的量比为1:2:3,因硝酸银浓度相同,则所用AgNO3溶液的体积比为1:2:3;若AgNO3的物质的量相等,则等浓度的NaC1、MgCl2、A1Cl3三种溶液中Cl﹣的物质的量相等,设NaC1、MgCl2、A1Cl3三种溶液浓度都是cmol/L,体积分别为xL、yL、zL,可得xc=2yc=3zc,整理的x:y:z=6:3:2,
故答案为:1:2:3;6:3:2;
(3)氢氧化钡是强电解质,所以在没加硫酸之前,氢氧化钡溶液具有一定导电能力,向Ba(OH)2溶液中逐滴加入稀硫酸,发生的反应为:H2SO4+Ba(OH)2=BaSO4↓+2H2O,随着氢氧化钡溶液的滴加,离子浓度逐渐减小,导电性逐渐降低,最后导电能力为零,也就是说恰好完全反应时没有自由移动的离子了,当硫酸过量时,溶液中自由移动的离子浓度逐渐增大,导电能力逐渐增大,直到和原来接近,所以溶液中溶液的导电性变化是强→弱(水有微弱的导电性)→强,曲线C符合导电性的变化趋势,
故答案为:C.
点评: 本题考查较综合,涉及离子共存、离子反应计算及图象等,为高频考点,把握常见离子之间的反应、离子反应中物质的量的关系及反应与图象的对应关系为解答的关键,侧重分析与应用能力的综合考查,题目难度不大.


 寒假学与练系列答案
寒假学与练系列答案科目:高中化学 来源: 题型:
X、Y、Z三种元素的原子,其最外层电子排布分别为ns1、3s23p1和2s22p4,由这三种元素组成的化合物的化学式可能是()
A. XYZ2 B. X2YZ3 C. X2YZ2 D. XYZ3
查看答案和解析>>
科目:高中化学 来源: 题型:
在含Mg2+、Al3+、H+、Cl﹣的混合溶液中滴加NaOH溶液,与OH﹣发生反应的顺序为: 、 、Mg2+和 .在NaOH滴加过量后的澄清溶液中,浓度最高的离子是 .
查看答案和解析>>
科目:高中化学 来源: 题型:
室温下将浓度相同的NaOH和HCl溶液以3:2体积比相混合,所得溶液的pH等于12,则原溶液的浓度为()
A. 0.01mol•L﹣1 B. 0.017mol•L﹣1 C. 0.05mol•L﹣1 D. 0.50mol•L﹣1
查看答案和解析>>
科目:高中化学 来源: 题型:
据报道,摩托罗拉公司开发了一种以甲醇为原料,以KOH为电解质的用于手机的可充电的高效燃料电池,充一次电可连续使用一个月.如图是一个电化学过程的示意图.已知甲池的总反应式为:2CH3OH+3O2+4KOH 2K2CO3+6H2O请填空:
2K2CO3+6H2O请填空:
(1)充电时:①原电池的负极与电源负极相连.②阳极的电极反应式为 .
(2)放电时:负极的电极反应式为 .
(3)在此过程中若完全反应,乙池中A极的质量升高648g,则甲池中理论上消耗O2 L(标准状况下).
(4)若在常温常压下,1gCH3OH燃烧生成CO2和液态H2O时放热22.68kJ,表示该反应的热化学方程式为 .
查看答案和解析>>
科目:高中化学 来源: 题型:
X、Y、Z、W四种短周期元素在周期表中相对位置如下表所示,Y是地壳中含量最高的元素.下列说法中不正确的是()
X Y
Z W
A. Z的原子半径大于Y
B. Y的非金属性强于W
C. W的氧化物对应的水化物都是强酸
D. X、Z的最高价氧化物均可与NaOH溶液反应
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com