
下列物质的类别与所含官能团都正确的是()
A. 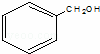
酚类﹣OH B. 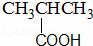
羧酸﹣COOH
C. 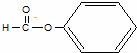
醛类﹣CHO D. CH3﹣O﹣CH3 酮类
考点: 烃的衍生物官能团.
专题: 有机化学基础.
分析: A.羟基与苯环侧链的C相连,属于醇类;
B.羧基与烃基直接相连,属于饱和一元羧酸;
C.该有机物分子中含有酯基,属于酯类;
D.C﹣O﹣C为 醚基,属于醚类.
解答: 解:A.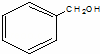 为苯甲醇,羟基不与苯环直接相连,不属于酚类,故A错误;
为苯甲醇,羟基不与苯环直接相连,不属于酚类,故A错误;
B.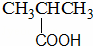 分子中含有羧基,属于羧酸类,故B正确;
分子中含有羧基,属于羧酸类,故B正确;
C. 为含有酯基,属于酯类,不属于醛类,故C错误;
为含有酯基,属于酯类,不属于醛类,故C错误;
D. 中含有醚基,属于醚类,不属于酮类,故D错误;
中含有醚基,属于醚类,不属于酮类,故D错误;
故选B.
点评: 本题考查了常见有机物官能团类型与分类方法判断,题目难度不大,注意掌握常见官能团结构及性质,明确有机物类型与含有的官能团的关系.


 新课标同步训练系列答案
新课标同步训练系列答案 一线名师口算应用题天天练一本全系列答案
一线名师口算应用题天天练一本全系列答案科目:高中化学 来源: 题型:
下述实验不能达到预期目的的是
| 选项 | 实验目的 | 实验方案 |
| A | 验证Ksp(AgCl)>Ksp(AgI) | 向NaCl溶液中滴加少量AgNO3溶液,产生白色沉淀,再滴加KI溶液,可观察到白色沉淀转化为黄色沉淀 |
| B | 检验Fe(NO3)2晶体是否已氧化变质 | 将Fe(NO3)2样品溶于稀H2SO4后,滴加KSCN溶液,观察溶液是否变红 |
| C | 验证Br2的氧化性强于I2 | 将少量溴水加入KI溶液中,再加入CCl4,振荡,静置。可观察到下层液体呈紫色 |
| D | 比较确定铜和镁的金属活动性强弱 | 用石墨作电极电解Mg(NO3)2、Cu(NO3)2的混合液 |
查看答案和解析>>
科目:高中化学 来源: 题型:
A、B、D、E、F为短周期元素,非金属元素A最外层电子数与其周期数相同,B的最外层电子数是其所在周期数的2倍。B在D中充分燃烧能生成其最高价化合物BD2。E+与D2- 具有相同的电子数。A在F中燃烧,产物溶于水得到一种强酸。回答下列问题:
(1)A在周期表中的位置是________,写出一种工业制备单质F的离子方程式______________________________________________________________。
(2)B、D、E组成的一种盐中,E的质量分数为43%,其俗名为________,其水溶液与F单质反应的化学方程式为________________________;在产物中加入少量KI,反应后加入CCl4并振荡,有机层显________色。
(3)由这些元素组成的物质,其组成和结构信息如下表:
| 物质 | 组成和结构信息 |
| a | 含有A的二元离子化合物 |
| b | 含有非极性共价键的二元离子化合物,且原子数之比为1∶1 |
| c | 化学组成为BDF2 |
| d | 只存在一种类型作用力且可导电的单质晶体 |
a的化学式为________;b的化学式为________;c的电子式为________;d是________。
查看答案和解析>>
科目:高中化学 来源: 题型:
有四种不同堆积方式的金属晶体的晶胞如图所示,有关说法正确的是()
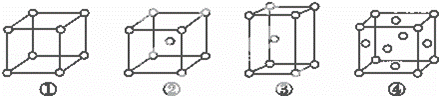
A. ①为简单立方堆积②为六方最密堆积③为体心立方堆积④为面心立方最密堆积
B. 每个晶胞含有的原子数分别为:①1个,②2个,③2个,④4个
C. 晶胞中原子的配位数分别为:①6,②8,③8,④12
D. 空间利用率的大小关系为:①<②<③<④
查看答案和解析>>
科目:高中化学 来源: 题型:
下面的排序不正确的是()
A. 晶体熔点由低到高:CH4<SiH4<GeH4<SnH4
B. 熔点由高到低:Rb>K>Na
C. 硬度由大到小:金刚石>碳化硅>晶体硅
D. 晶格能由大到小:NaF>NaCl>NaBr>NaI
查看答案和解析>>
科目:高中化学 来源: 题型:
A、X、Y、Z、R、W均为周期表中前四周期的元素,其中原子序数依次增大;A原子价电子排布式nsnnpn+1,X2﹣和Y+有相同的核外电子排布;Z的气态氢化物的沸点比其上一周期同族元素气态氢化物的沸点低;R的基态原子在前四周期元素的基态原子中单电子数最多;W为金属元素,X与W形成的某种化合物与Z的氢化物的浓溶液加热时反应可用于实验室制取Z的气体单质.回答下列问题(相关回答均用元素符号表示):
(1)R基态原子的核外电子排布式是 .W在周期表中的位置是
(2)NH4Cl晶体中含有多种化学键,其中一定不含有的化学键是 (填字母).
A.离子键B.极性键C.配位键 D.金属键
(3)A原子的第一电离能 (填“大于”、“小于”或“等于”)X原子的第一电离能; A元素的氢化物是一种易液化的气体,该气体易液化的原因是
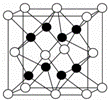
(4)X与Y形成的化合物Y2X2的电子式 ,其晶体类型是 .X与Y形成的化合物的晶胞如图所示,则该化合物的化学式为 (请用推断出的元素符号表示).
(5)Z的某种含氧酸盐常用于实验室制取X形成的单质,此酸根离子的空间构型为 .
查看答案和解析>>
科目:高中化学 来源: 题型:
某酯分子式为C6H12O2,该酯水解生成A和B,B是A的同分异构体的氧化产物,该酯为( )
|
| A. | CH3CH(CH3)COOC2H5 | B. | CH3CH2COO(CH2)2CH3 |
|
| C. | CH3COO(CH2)3CH3 | D. | CH3CH2COOCH(CH3)2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
NH3经一系列反应可以得到HNO3和NH4NO3,如下图所示。

(1)Ⅰ中,NH3和O2在催化剂作用下反应,其化学方程式是_________________________。
(2)Ⅱ中,2NO(g)+O2(g)  2NO2(g)。在其他条件相同时,分别测得NO的平衡转化率在不同压强(p1、p2)下随温度变化的曲线(如图)。
2NO2(g)。在其他条件相同时,分别测得NO的平衡转化率在不同压强(p1、p2)下随温度变化的曲线(如图)。
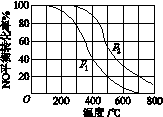
①比较p1、p2的大小关系:________。
②随温度升高,该反应平衡常数变化的趋势是________。
(3)Ⅲ中,降低温度,将NO2(g)转化为N2O4(l),再制备浓硝酸。
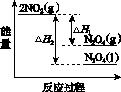
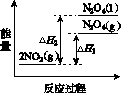
①已知:2NO2(g)  N2O4(g) ΔH1 2NO2(g)
N2O4(g) ΔH1 2NO2(g) N2O4(l) ΔH2
N2O4(l) ΔH2
下列能量变化示意图中,正确的是(选填字母)________。

A B C
②N2O4与O2、H2O化合的化学方程式是________________________________________。
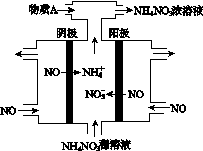
(4)Ⅳ中,电解NO制备NH4NO3,其工作原理如图所示。为使电解产物全部转化为NH4NO3,需补充A。A是________,说明理由:________________________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com