
【题目】某温度下,在容积固定的密闭容器中充入CH4、CO2 发生此反应![]() ,下列选项可说明上述反应达到平衡状态的是( )。
,下列选项可说明上述反应达到平衡状态的是( )。
A. 混合气体的密度不再发生变化B. 混合气体的平均相对分子质量不再发生变化
C. 混合气体的总质量不再发生变化D. 相同时间内每断开2mol C=O键,同时断开1mol H-H键
【答案】B
【解析】
A.参加反应的均为气体,反应前后气体的质量不变,气体的体积不变,故气体的密度始终不变,故当混合气体的密度不再发生变化时不能说明反应达平衡,故A错误;
B.混合气体的质量不变,但物质的量增大,故混合气体的平均相对分子质量逐渐变小,故当混合气体的平均相对分子质量不变时能说明反应达平衡,故B正确;
C.参加反应的均为气体,反应前后气体的质量始终不变,故当混合气体的总质量不再发生变化时不能说明反应达平衡,故C错误;
D.相同时间内每断开2mol C=O键即消耗1mol二氧化碳,同时断开1mol H-H键即消耗1mol氢气,则表示正反应速率>逆反应速率,不是平衡状态,故D错误;
答案选B。


 百分学生作业本题练王系列答案
百分学生作业本题练王系列答案 互动课堂系列答案
互动课堂系列答案科目:高中化学 来源: 题型:
【题目】某离子反应中涉及H2O、ClO-、NH4+、H+、N2、Cl-六种粒子。其中N2、ClO-的物质的量随时间变化的曲线如图所示。下列判断不正确的是

A. 该反应的氧化剂是ClO-
B. 消耗1mol还原剂,转移3mol电子
C. 氧化剂与还原剂的物质的量之比为2:3
D. 该离子方程式为3ClO-+2NH4+=2H++N2↑+3Cl-+3H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】利用海洋资源获得的部分物质如图所示.下列说法正确的是
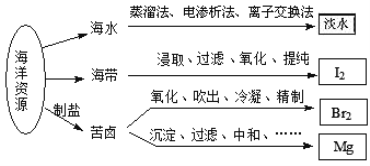
A. 从海水中获取淡水,历史最久的方法是离子交换法
B. 实验室中从海带中获得I2,需要用到的主要仪器有蒸发皿、漏斗、烧杯、分液漏斗等
C. 用Na2CO3溶液吸收从苦卤中吹出的单质溴时,发生的化学反应可以是3Br2+3Na2CO3═5NaBr+ NaBrO3+3CO2或3Br2+6Na2CO3+3H2O═5NaBr+NaBrO3+6NaHCO3
D. 用贝壳、盐酸等从苦卤中提取镁时,发生反应的类型有化合、分解、置换和复分解
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】关于原电池的说法正确的是( )
A.电流从原电池的负极流向正极
B.电子从发生还原反应的电极流出
C.原电池是将化学能转变为电能的一种装置
D.原电池的两个电极,一定是由活动性不同的两种金属组成
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】镁原子电池放电时电压高而平稳,电池反应为xMg + Mo3S4 ![]() MgxMo3S4,下列说法错误的是
MgxMo3S4,下列说法错误的是
A. 放电时负极反应为Mg-2e-===Mg2+
B. 充电时阳极反应为Mo3S4+xMg2++2xe-===MgxMo3S4
C. 放电时Mg2+向正极区移动
D. 充电时电池的负极接充电电源的负极
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业上以氧化铝为原料可制得一些物质。
(1)碳热还原法可合成氮化铝(AlN)
已知:2Al2O3(s)==4Al(g)+3O2(g) △H1=+3351KJmol﹣1
2C(s)+O2(g)==2CO(g) △H2=-221KJmol﹣1
2Al(g)+N2(g)==2AlN(s) △H3=-318KJmol﹣1
碳热还原Al2O3合成AlN的总热化学方程式是________________________________________________,
(2)电解法可制取铝。以石墨作电极电解熔融 Al2O3(加入Na3AlF6为助熔剂)
①电解时铝在_____________产生(填阴极或阳极)
②电解过程中作阳极的石墨易消耗,原因是________________________。
(3)二氧化碳甲烷化再利用
①已知反应:CO2(g)+4H2(g)![]() CH4(g)+2H2O(g)写出该反应的平衡常数表达式________________________
CH4(g)+2H2O(g)写出该反应的平衡常数表达式________________________
②据文献报道,CO2可以在碱性水溶液中电解生成甲烷,生成甲烷的电极反应式是_________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】图中A为淡黄色固体,B的阳离子与A相同(其他物质均略去).
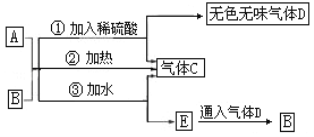
根据以上关系,回答下列问题:
(1)A的电子式为__________.
(2)A投入FeCl2溶液中的反应为_______________(请用一个化学方程式表示)
(3)若A、B按物质的量之比1:1.5混合在密闭容器中加热充分反应后,排出气体,则剩余的固体为_____________________________(写化学式)
(4)氢能被视为21世纪最具发展潜力的清洁能源,试回答下列问题:
①与化石燃料相比,氢气作为燃料的优点是__________________(答两点)。
②施莱辛(Sehlesinger)等人提出可用NaBH4与水反应制氢气,写出NaBH4与水反应的化学方程式____________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为了研究碳酸钙与盐酸反应的反应速率,某同学通过实验测定碳酸钙固体与足量稀盐酸反应生成CO2的体积随时间的变化情况,绘制出下图所示的曲线甲。下列有关说法中不正确的是

A. 在0-t1、t1-t2、t2-t3中,t1-t2生成的CO2气体最多
B. 因反应放热,导致0-t1内的反应速率逐渐增大
C. 若用单位时间内CO2的体积变化来表示该反应的速率,则t2-t3时间内平均反应速率为![]() mLs-1
mLs-1
D. 将碳酸钙固体研成粉末,则曲线甲将变成曲线乙
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A是来自石油的重要有机化工原料,此物质可以用来衡量一个国家石油化工发展水平。E是具有果香味的有机物,D能与碳酸钠反应产生气体,F是一种高聚物,可制成多种包装材料。
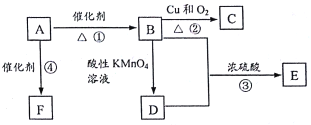
(1)A的结构式为___________。
(2)C分子中的官能团名称是_________,验证C物质存在该官能团的试剂是__________,现象为_________________________。
(3)写出下列反应的化学方程式并指出反应类型:
①____________________________:反应类型是______________;
③____________________________;反应类型是______________;
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com