
��ǿ����ǿ���ϡ��Һ�����кͷ�Ӧ����ЧӦΪ��H+(aq) +OH-(aq)�TH2O(l)
��H = -57��3kJ/mol���ֱ���1L 0��5mol/L��Ba(OH)2����Һ�м����Ũ����� ϡ�����ϡ���ᣬǡ����ȫ��Ӧ����ЧӦ�ֱ�Ϊ��H1����H2����H3�����й�ϵ��ȷ����
| A����H1����H2����H3 | B����H1����H2����H3 |
| C����H1����H2����H3 | D����H1����H2����H3 |
 �������Ӧ���⼯ѵϵ�д�
�������Ӧ���⼯ѵϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
SF6��һ�������ľ�Ե���壬���ӽṹ��ֻ����S��F������֪��1 mol S(s)ת��Ϊ��̬��ԭ����������280 kJ������1 mol F��F��S��F�������յ������ֱ�Ϊ160 kJ��330 kJ����S(s)��3F2(g)=SF6(g)�ķ�Ӧ�Ȧ�HΪ(����)
| A����1 780 kJ��mol��1 | B����1 220 kJ��mol��1 |
| C����450 kJ��mol��1 | D����430 kJ��mol��1 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
��֪��C(s��ʯī) ="=" C(s�����ʯ) ��H =" +1.9" kJ��mol-1�������й�˵����ȷ����
| A����ͬ�����£�1 molʯī��1 mol���ʯ������ |
| B������1molʯī�еĻ�ѧ�����յ������ȶ���1mol���ʯ�еĻ�ѧ�����յ������� |
| C������C(s��ʯī) + O2(g)==CO2(g) ��H1=��393.5 kJ?mol-1 ���У�C(s�����ʯ) + O2(g)==CO2(g)��H2=��395.4 kJ��mol-1 |
| D��������������ʱ��������ʵĴ�������ʵ�ָ÷�Ӧ�ķ�Ӧ��ת��Ϊ��H��0 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
��ѧ��Ӧ��ͨ�������������仯������˵���д������
| A��úȼ��ʱ�����ֻ�ѧ��ת��Ϊ���� |
| B���������Al2O3ʱ�����ֻ�ѧ��ת��Ϊ���� |
| C��TNT��ըʱ�����ֻ�ѧ��ת��Ϊ���� |
| D��þ��ȼ��ʱ�����ֻ�ѧ��ת��Ϊ���� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
��ӦCO(g)��2H2(g)  CH3OH(g)�����е������仯�������ͼ��ʾ�����ߢ�����ߢ�ֱ��ʾ��ʹ�ô�����ʹ�ô�������������������ж���ȷ����
CH3OH(g)�����е������仯�������ͼ��ʾ�����ߢ�����ߢ�ֱ��ʾ��ʹ�ô�����ʹ�ô�������������������ж���ȷ����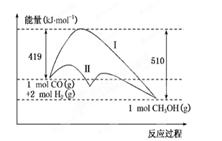
| A���÷�Ӧ�Ħ�H����91 kJ/mol |
| B����������������淴Ӧ�Ļ����ֵ����С |
| C������������÷�Ӧ�Ħ�H��С |
| D������÷�Ӧ����Һ̬CH3OH����H��� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
�������������Ȼ�ѧ����ʽ��
��1��2H2S(g)+3O2(g)=2SO2(g)+2H2O(l) ��H= -Q1kJ��mol-1
��2��2H2S(g)+O2(g)=2S(g)+2H2O(g) ��H= -Q2kJ��mol-1
��3��2H2S(g)+O2(g)=2S(g)+2H2O(l) ��H= -Q3kJ��mol-1
�ж�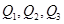 ���߹�ϵ��ȷ����
���߹�ϵ��ȷ����
| A��Q1��Q2��Q3 | B��Q1��Q3��Q2 | C��Q3��Q2��Q1 | D��Q2��Q1��Q3 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
���з�Ӧ�������ȷ�Ӧ����
| A��̼��ˮ������ˮú���ķ�Ӧ | B����ʯ�Һ�ˮ�ķ�Ӧ |
| C������������������Һ�ķ�Ӧ | D��ľ̿��������ȼ�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
����˵�����ʾ������ȷ����
| A�������ʵ�����������������ֱ���ȫȼ�գ����߷ų������� |
| B����C��ʯī���� C�����ʯ�� ��H����1.90 kJ/mol��֪�����ʯ��ʯī�ȶ� |
| C����101kPaʱ��2g������ȫȼ������Һ̬ˮ���ų�285.8kJ����������ȼ�յ��Ȼ�ѧ����ʽ��ʾΪ�� 2H2(g)+O2(g)��2H2O(l) ��H����285.8kJ/mol |
| D����ϡ��Һ�У�H+(aq)+ OH-(aq)��H2O(l) ��H����57.3kJ/mol��������0.5molH2SO4��Ũ�����뺬1molNaOH����Һ��ϣ��ų����ȴ���57.3kJ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
����˵����ȷ���ǣ� ��
| A����Ӧ�Ⱦ��Ƿ�Ӧ�зų������� |
| B����101 kPaʱ��1 mol̼ȼ�����ų�������Ϊ̼��ȼ���� |
| C���������������������ֱ���ȫȼ�գ�ǰ�߷ų��������� |
| D����C(ʯī)��C(���ʯ) ��H��+1.9 kJ��mol��1��֪�����ʯ��ʯī�ȶ� |
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com